
Instrumentation : SOLATION® ICP-MS
INTRODUCTION
Avec l'acceptation et la légalisation croissantes du chanvre et du cannabis aux États-Unis, au Canada et dans plusieurs autres pays, les produits à base de cannabis sont plus largement disponibles que jamais. Désormais approuvée pour les utilisations médicales, récréatives et de suppléments de santé, l'augmentation de la production et de la consommation a mis en évidence la nécessité de tests de routine et d'élaboration de normes de test pour les produits chimiques toxiques, y compris les métaux lourds, dans le matériel végétal de cannabis et tous les sous-produits qui en sont issus, afin de garantir produits sûrs pour le consommateur. Avec l'adoption des chapitres <232> et <233>, la pharmacopée américaine (USP) précise une liste d'éléments et de limites d'exposition maximales en fonction de la toxicité et des voies d'administration des produits pharmaceutiques.
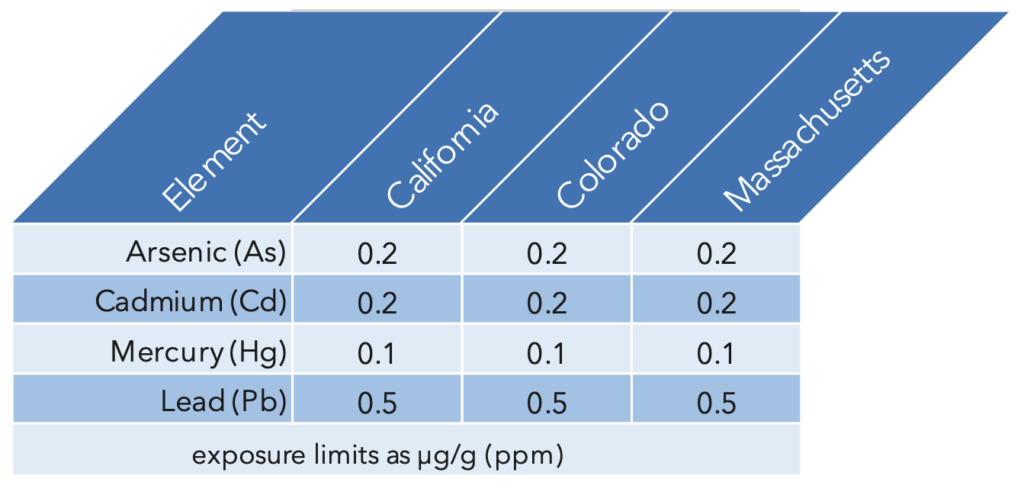
De nombreux États qui ont légalisé le cannabis médical et récréatif fondent leurs limites d'exposition sur les valeurs USP. La Californie, le Colorado et le Massachusetts sont des exemples de limites d'exposition quotidienne admissible (PDE) par inhalation pour l'As, le Cd, le Hg et le Pb. Ces valeurs sont résumées dans le tableau 1.
Tableau 1: Limites de PDE pour les États qui utilisent les directives de l'USP pour l'exposition aux métaux lourds par inhalation. USP<233> définit également la précision, la répétabilité et la robustesse requises pour l'analyse de ces éléments toxiques :
![]() Critères de validation
Critères de validation
Exactitude: La matrice et les matériaux à l'étude doivent être enrichis d'éléments cibles à des concentrations de 50 %, 100 % et 150 % de l'exposition quotidienne maximale autorisée (PDE). Les récupérations de pointe moyennes pour chaque élément cible doivent être comprises entre 70 % et 150 % de la valeur réelle.
Répétabilité: Six échantillons indépendants du matériau à l'étude doivent être dopés à 100 % des limites cibles définies et analysées. Le pourcentage d'écart type relatif mesuré (%RSD) ne doit pas dépasser 20 % pour chaque élément cible.
Rugosité: Effectuer la procédure de test de mesure de répétabilité en analysant les six solutions de test de répétabilité soit à des jours différents, soit avec un instrument différent, soit par un analyste différent. Le %RSD des 12 réplicats doit être inférieur à 25 % pour chaque élément cible.
Dans cette étude, nous avons utilisé le Advion SOLATION® ICP-MS et un système de digestion par micro-ondes pour digérer et analyser des échantillons de chanvre à l'aide des méthodes de validation décrites dans le chapitre général de l'USP <233>. La sensibilité, la capacité à gérer des matrices complexes et la capacité à éliminer les interférences avec une cellule de collision à l'hélium en font le système idéal pour l'analyse des métaux lourds dans l'industrie du cannabis.
EXPÉRIENCE
La préparation des échantillons
Un échantillon de fleur de chanvre médicinal a été acheté localement. Environ 14 grammes ont été finement broyés et homogénéisés, puis 0.5 g +/- 0.005 g ont été pesés dans des récipients de digestion et la quantité appropriée d'une solution de pointe ajoutée. Neuf ml de HNO3 concentré et 1 ml de HCl concentré ont été ajoutés à chaque récipient et les échantillons ont été laissés réagir pendant 15 minutes avant de sceller et de placer les récipients sur le plateau tournant du système de digestion par micro-ondes à récipient fermé. Le programme contrôle l'énergie des micro-ondes de manière à ce que les échantillons atteignent la température de digestion optimale de 200 °C en 20 minutes, maintiennent 200 °C pendant 10 minutes, puis refroidissent à température ambiante.
Cette méthode a abouti à la digestion complète de tous les échantillons résultant en une solution claire et sans particules une fois portée au volume avec de l'eau 18 MΩ dans une fiole jaugée de 50 ml.
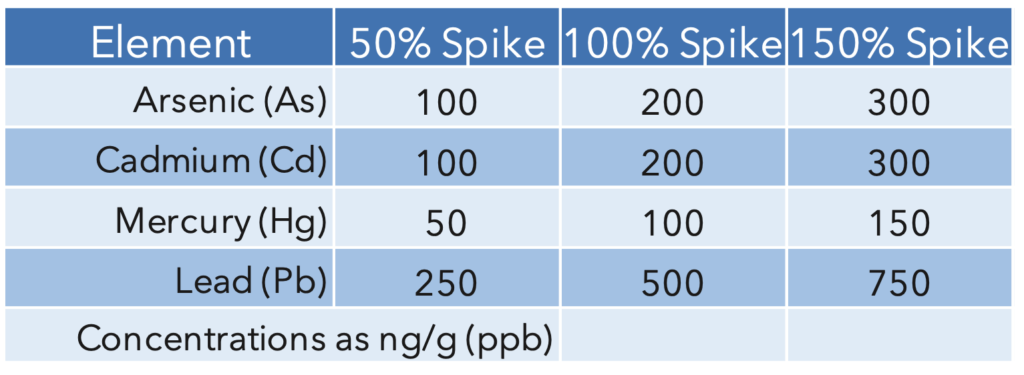
Les normes d'étalonnage et les pointes étaient basées sur les niveaux d'action du tableau 1. L'ensemble d'échantillons comprenait un échantillon de chanvre, un duplicata, les pointes à 50 %, 100 % et 150 % et des aiguilles de pin NIST 1575 pour valider davantage les résultats, qui ont été exécutés en double. Pour la spécification de « rugosité » de l'USP<233>, il y avait 6 échantillons de chanvre dopé à 100 %. Les valeurs de pointe sont résumées dans le tableau 2.
Tableau 2: Valeurs de pointe basées sur les limites d'action définies dans l'USP<233>
![]()
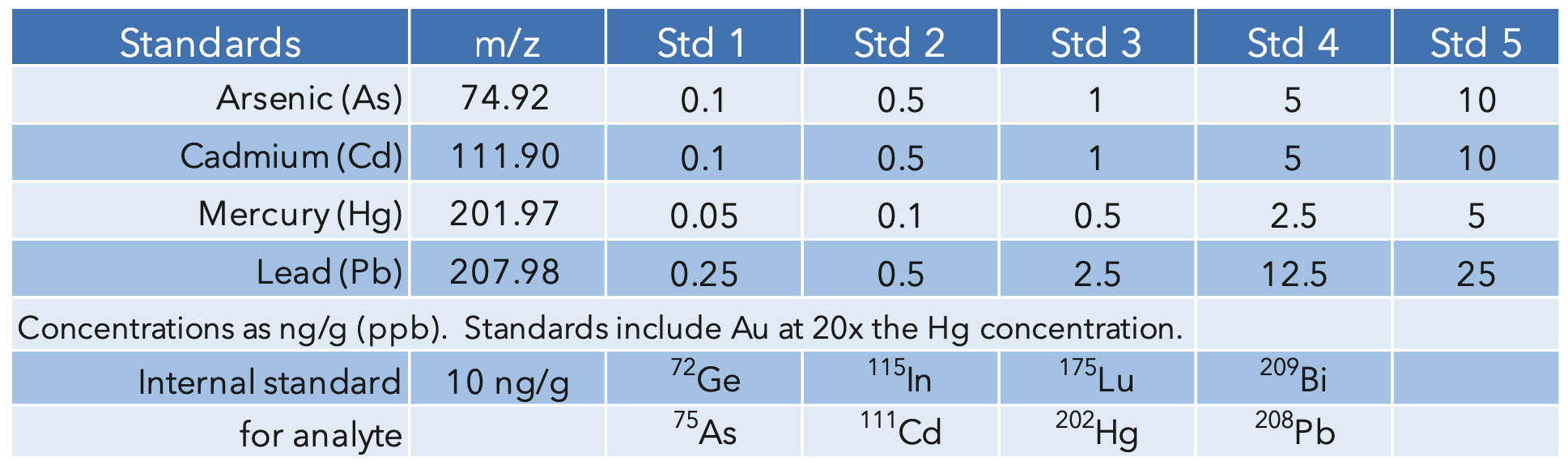
Une seconde dilution 1:4 a été effectuée après la digestion pour amener la concentration finale en acide à 5 % pour un facteur de dilution global de 400x. Le blanc d'étalonnage et les standards ont été préparés en utilisant la même concentration d'acide, 5% de 9:1 HNO3/HCl, pour l'appariement matriciel. Pour stabiliser le mercure et aider au lessivage, de l'or a été ajouté à 20 fois la concentration de mercure. Les standards internes ont été ajoutés à tous les échantillons, standards et blancs pour une concentration finale de 10 ng/g (ppb). Les concentrations étalons et les étalons internes sont résumés dans le tableau 3.
Tableau 3: Masses d'analytes, étalons d'étalonnage et étalons internes.
Instrumentation
L'Advion SOLATION® ICP-MS intègre un générateur à semi-conducteurs robuste, une optique ionique orthogonale pour garder les composants les plus sensibles de MS propres et un logiciel de contrôle et de traitement des données facile à utiliser.
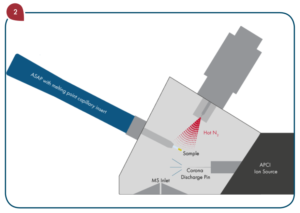
Comme HCl a été utilisé dans la digestion de l'échantillon, il y a une quantité importante de chlore présent qui crée une interférence isobare sur 75À partir 40Ar35Cl+. La cellule de collision élimine efficacement la contribution que ArCl+ apporte au signal à m/z 75 en tirant parti de la discrimination d'énergie cinétique (KED) pour séparer les interférences polyatomiques des ions analytes, ce qui permet une quantification précise des faibles niveaux d'arsenic. L'arsenic est le seul analyte de la suite avec ce type d'interférence, donc la cellule de collision n'est pas utilisée pour le Cd, le Hg ou le Pb.
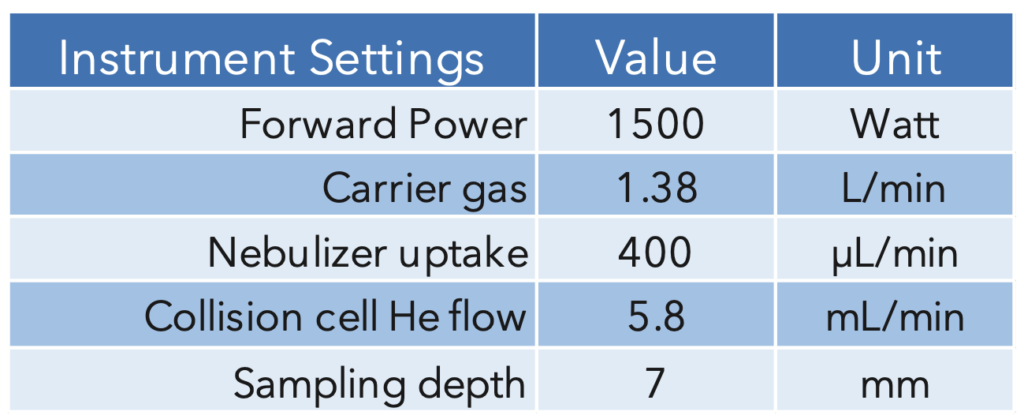
Un nébuliseur concentrique en verre monté sur une chambre de nébulisation cyclonique, connecté à la torche standard avec un diamètre d'injecteur de 2 mm, a été utilisé pour l'introduction de l'échantillon. Les paramètres de fonctionnement de l'instrument sont résumés dans le tableau 4.
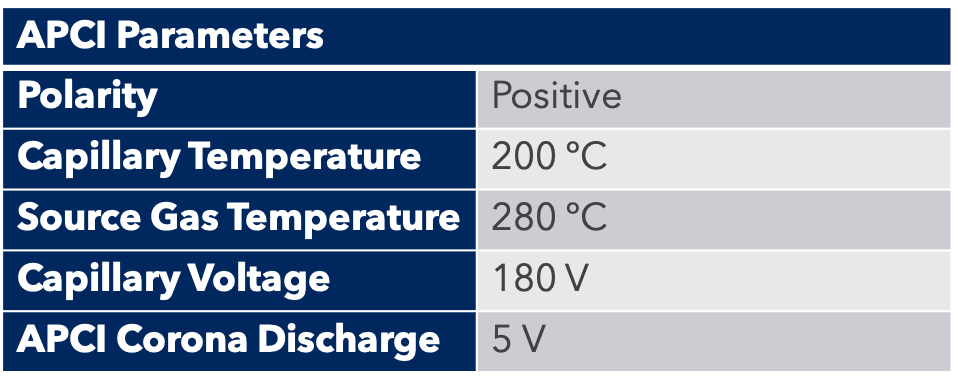
Tableau 4: Paramètres ICP-MS
RÉSULTATS ET VALIDATION
Exemples de résultats![]()
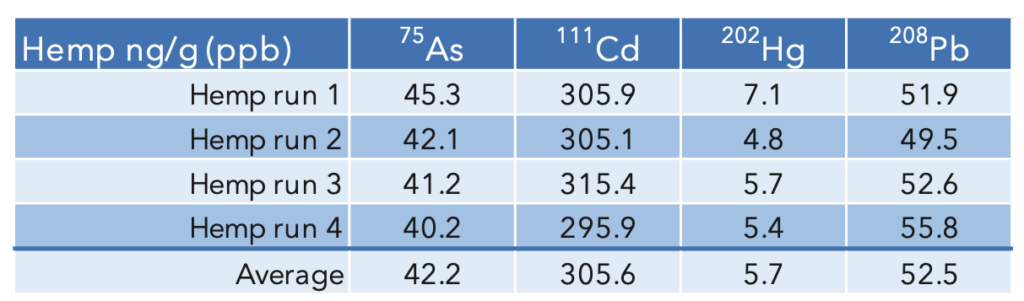
Les concentrations de mercure et de plomb dans le chanvre étaient inférieures à la norme la plus basse et toutes les valeurs étaient inférieures aux limites d'action. Les échantillons ont été préparés et analysés en double, et la moyenne de ces doubles est indiquée dans le tableau 5. Conformément à l'exigence de robustesse, les échantillons ont été analysés à des jours différents par deux analystes différents.
Tableau 5: Résultats de l'échantillon de chanvre (moyenne de l'échantillon et duplicata)
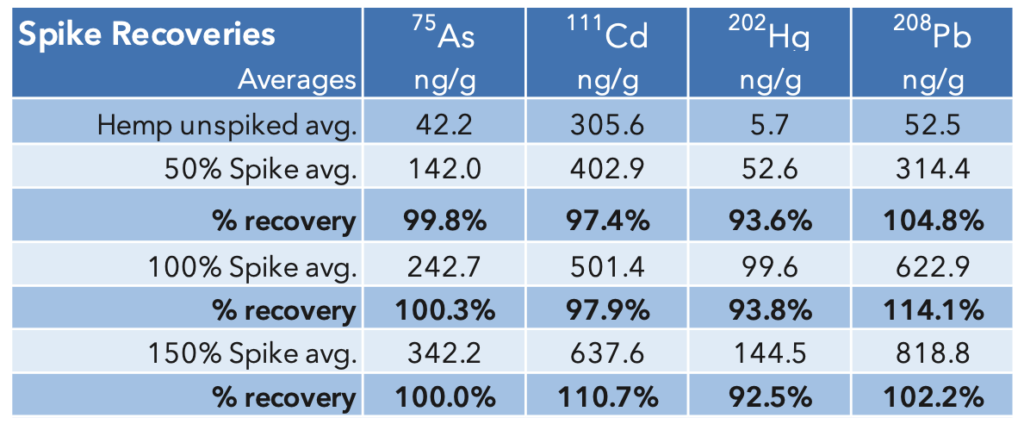
Exactitude: Les échantillons ont été enrichis à 50 %, 100 % et
150 % du niveau d'intervention (tableau 2 ci-dessus) et le pourcentage de récupération calculé. Les récupérations de pointes étaient toutes comprises entre 92.5% et 114.1%, bien dans la plage de 70 à 150 % définie par la méthode USP.
Tableau 6: Précision - récupérations de pointes
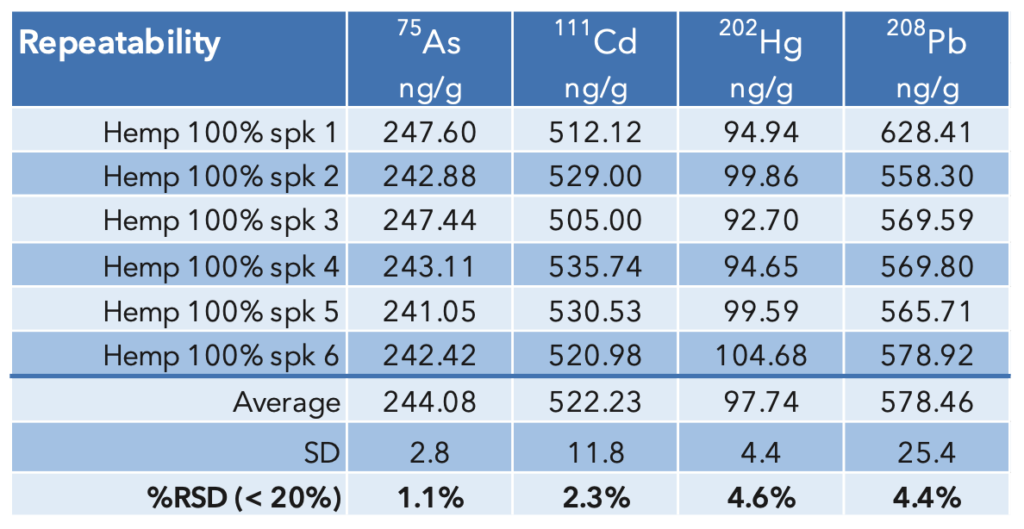
Répétabilité: Six échantillons de chanvre ont été dopés à 100 % du niveau d'action et digérés. Les résultats qui sont résumés dans le tableau 7 montrent que le %RSD des concentrations mesurées se situe entre 1.3 % et 3.7 %, démontrant une répétabilité bien inférieure à la limite de 20 %.
Tableau 7: USP<233> Résultats de répétabilité
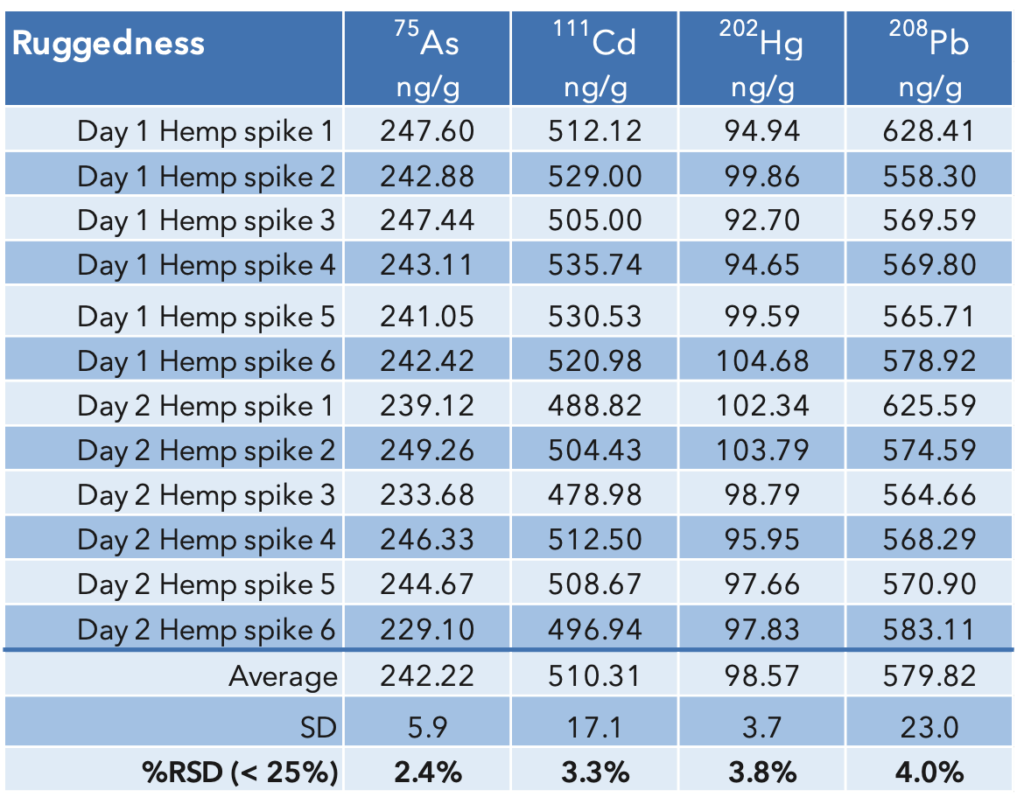
Rugosité: L'ensemble d'échantillons de répétabilité a été préparé et exécuté un autre jour par un autre analyste. Les résultats de cette exécution sont combinés avec l'exécution précédente pour déterminer la robustesse. Les valeurs de robustesse sont similaires aux valeurs de répétabilité et le %RSD mesuré (2.4 à 4.0 %) se situe confortablement sous la limite de 25 % définie par la méthode USP. Les résultats sont résumés dans le tableau 8.
Tableau 8: USP<233> Résultats de robustesse
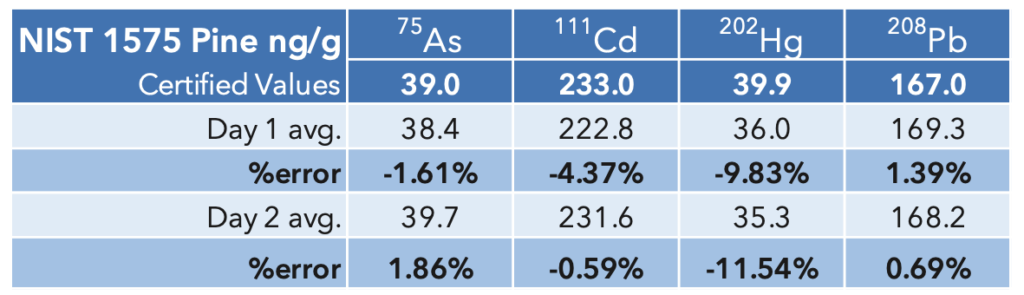
Résultats NIST 1575a
Les résultats du NIST SRM sont résumés dans le tableau 9. Les valeurs pour As et Hg étaient inférieures à
l'étalon bas en solution mais il y a un bon accord entre les valeurs expérimentales et les valeurs certifiées.
Tableau 9: NIST 1575a Aiguilles de pin SRM
CONCLUSION
Cette étude démontre que l'Advion SOLATION® ICP-MS, couplé à un système de digestion par micro-ondes, est adapté à l'analyse précise, robuste et reproductible des métaux lourds dans le matériel végétal de chanvre, dépassant largement les exigences du protocole USP <233>.
La validation de la méthode de digestion par micro-ondes a été renforcée par les excellents résultats de récupération obtenus pour le pin NIST SRM 1575.

























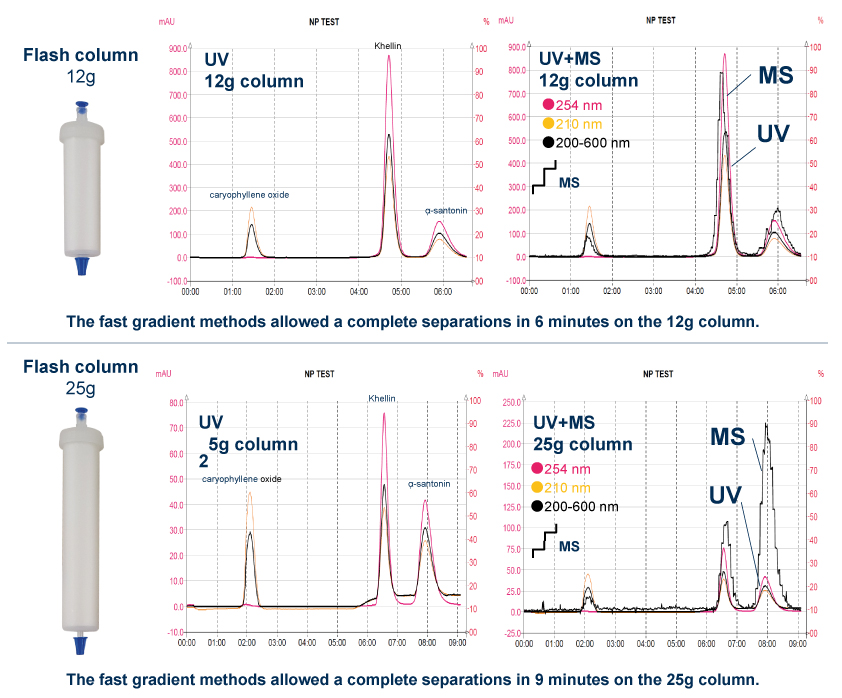
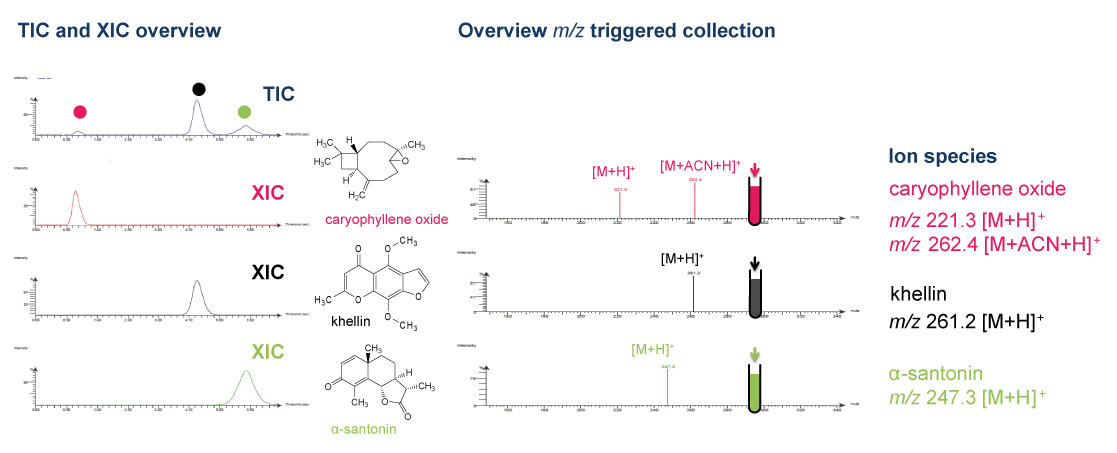
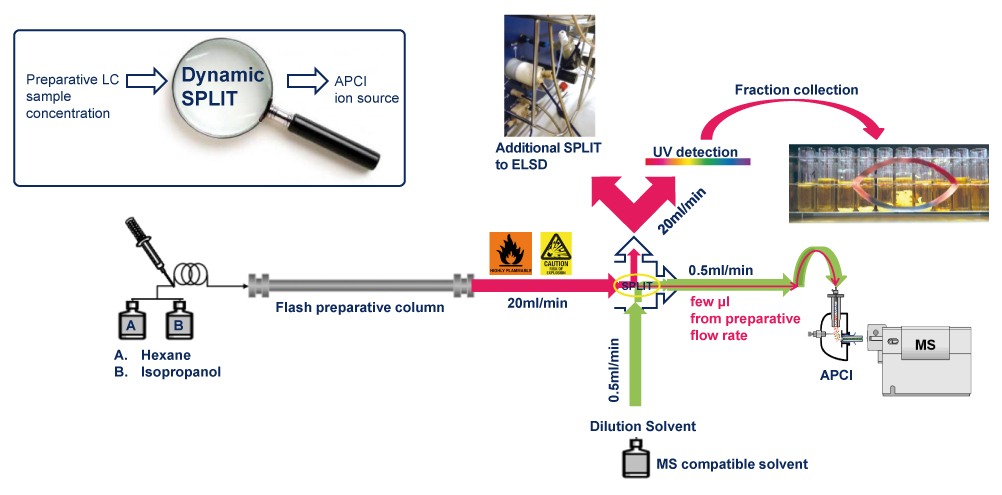
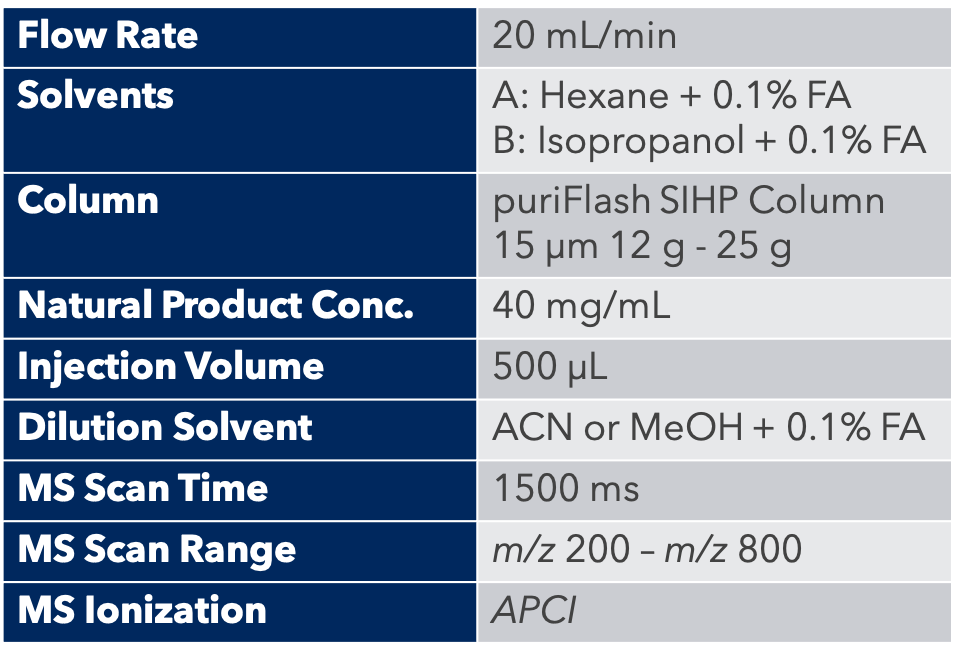





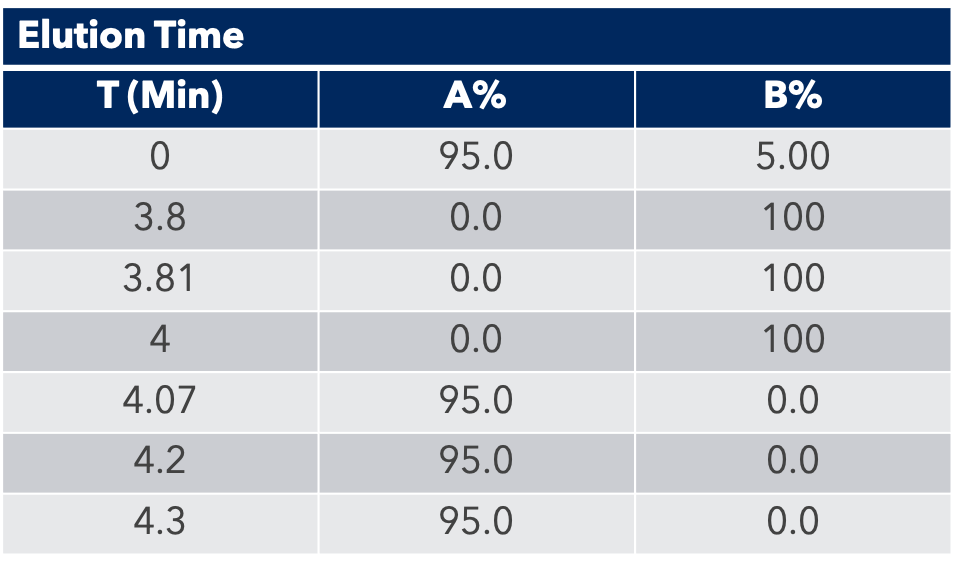
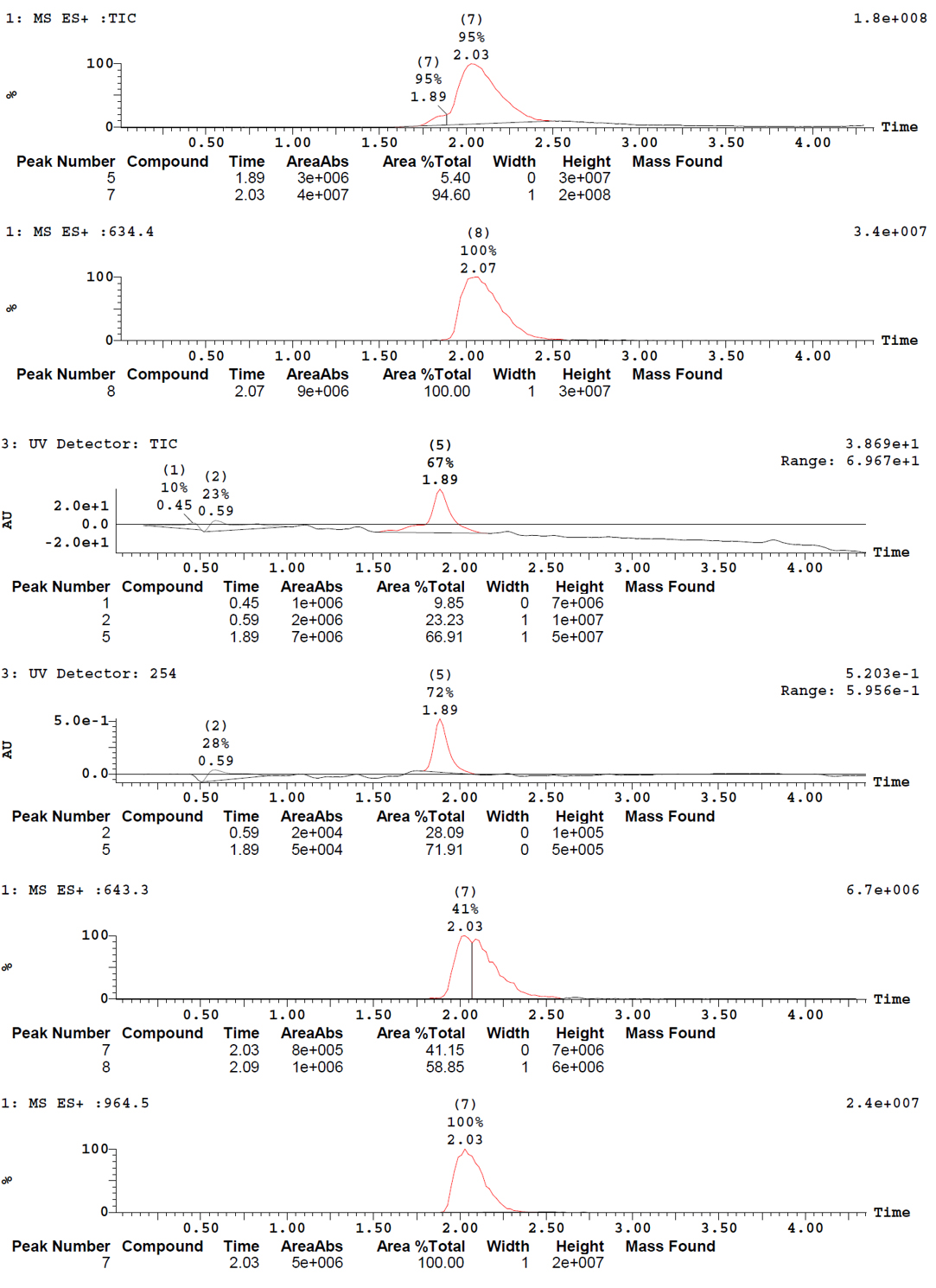
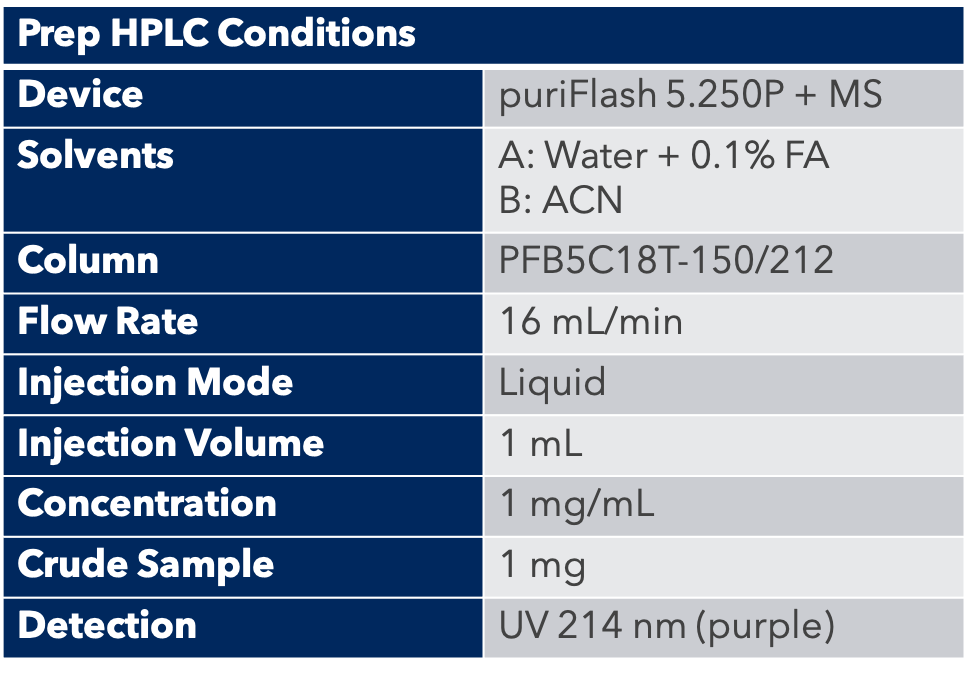
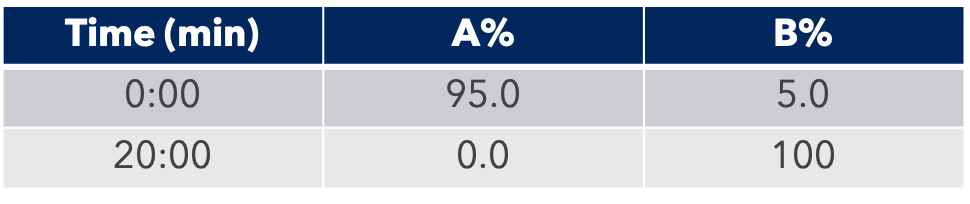
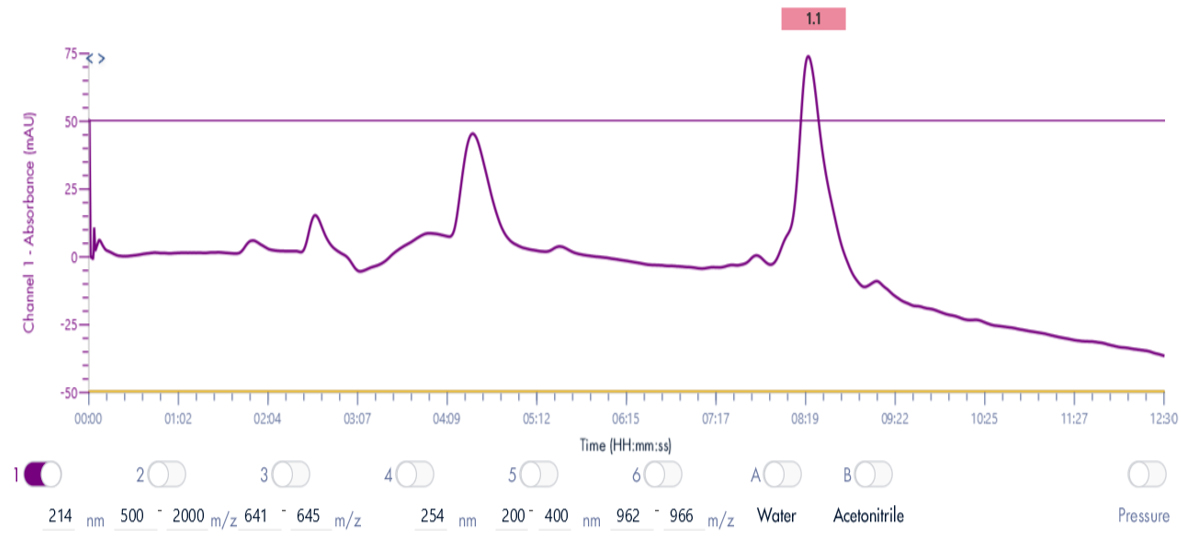
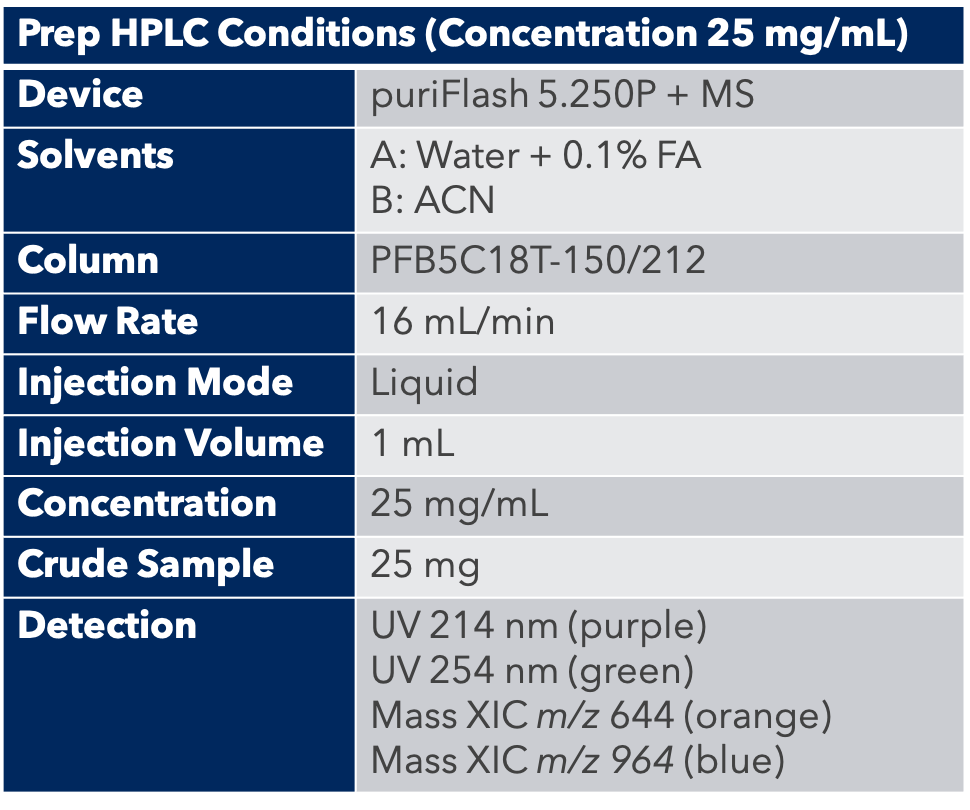
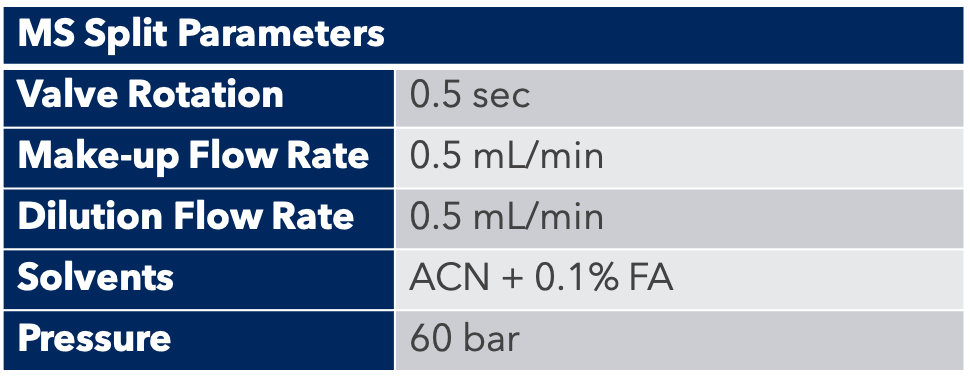
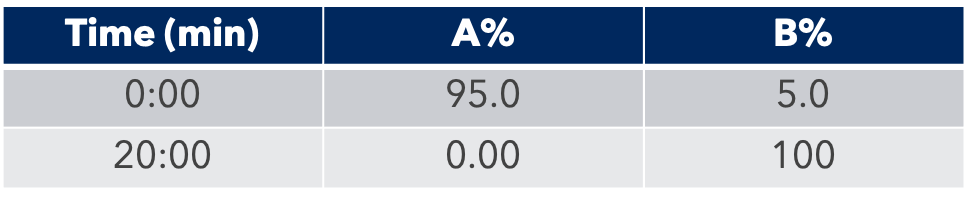
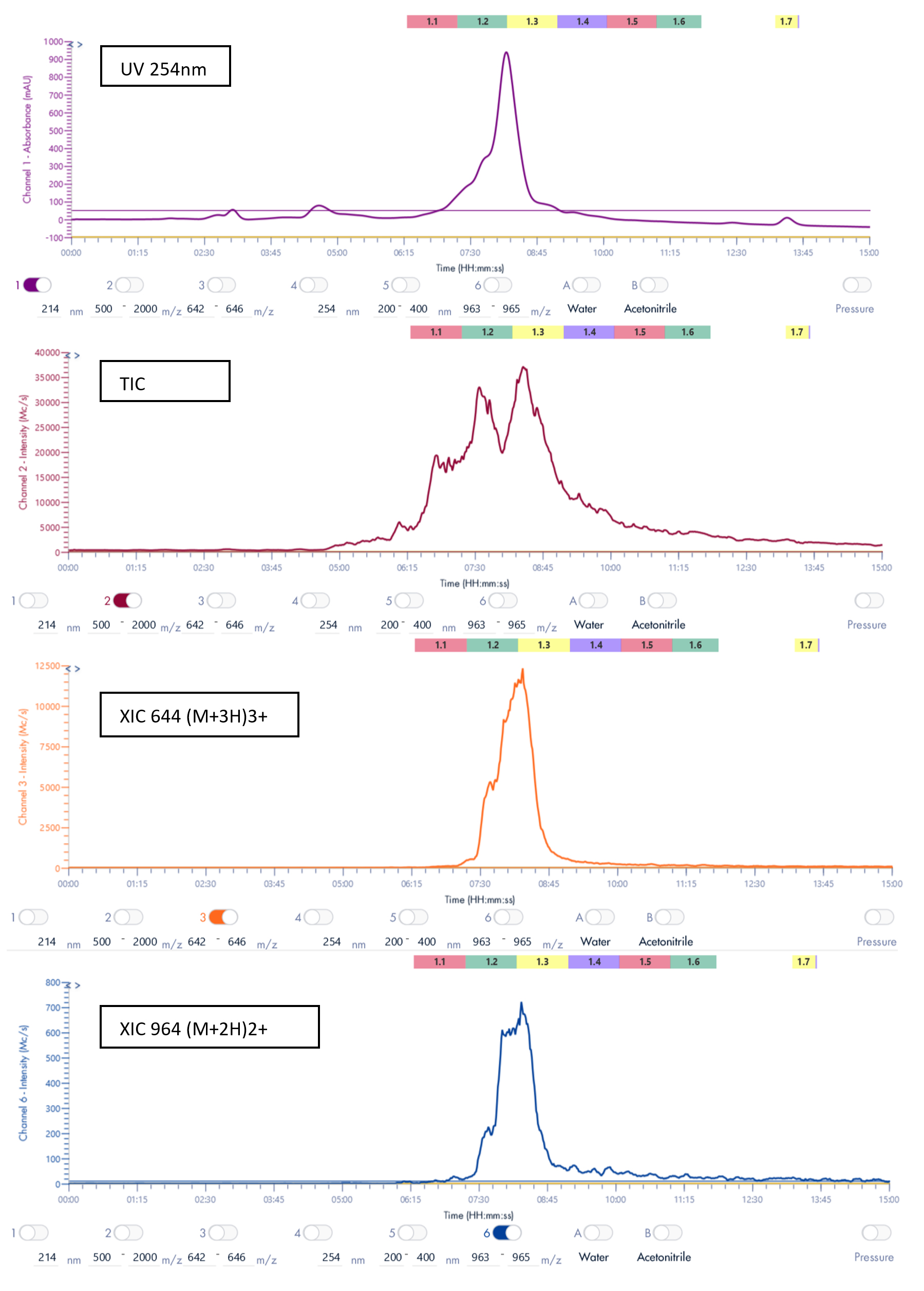 Grâce au système puriFlash 5.250P couplé à l'ex
Grâce au système puriFlash 5.250P couplé à l'ex