Qualitative Analyse von Oligonukleotiden mit Advion Interchim Scientific® HPLC-UV/MS-System

Anzeigen / Instrumente
Massenspektr: ExPresseIon® Kompaktes Massenspektrometer (CMS)
HPLC: AVANT®
Einführung
Oligonukleotide haben aufgrund ihrer Eigenschaften große Aufmerksamkeit in der biopharmazeutischen Entwicklung erlangt
Fähigkeit, die Gen- oder Proteinexpression zu modulieren. Ihr klinischer Erfolg zeigt sich in der Zulassung mehrerer Medikamente auf Oligonukleotidbasis oder in deren Einführung in klinische Studien.[1]. Zu diesen Medikamenten gehören Antisense-Oligonukleotide, Small Interfering RNA (siRNA)-Therapeutika und mRNA-basierte Impfstoffe, was durch die erfolgreiche Entwicklung von COVID-19-Impfstoffen veranschaulicht wird. Solche Erfolge haben weiteres Interesse und Investitionen in die Oligonukleotidforschung und -entwicklung geweckt.
Die Festphasensynthese ist eine häufig verwendete Methode zur Herstellung von Oligonukleotidsequenzen. Das Rohmaterial wird typischerweise durch verschiedene Techniken wie Entsalzung, Ultrafiltration, Festphasenextraktion (SPE), Hochleistungsflüssigkeitschromatographie (HPLC) oder präparative Flüssigkeitschromatographie (prepLC) gereinigt, je nach gewünschtem Reinheitsgrad. Ionenpaar-HPLC- oder PrepLC-Methoden werden häufig bevorzugt, da sie im Vergleich zu anderen Techniken eine höhere Reinheit bieten.
Ziel dieses Anwendungshinweises ist es, die HPLC/UV-Analyse mehrerer Oligoproben zu demonstrieren und die HPLC/CMS-Analyse zur Bestimmung ihres Molekulargewichts zu nutzen.
Methodik
HPLC-UV/CMS-System
Mit einer quaternären Pumpe und einem Säulenauswahlventil wird der Wechsel zwischen verschiedenen Puffern und Säulen für verschiedene Analysen bemerkenswert einfach, sodass keine manuelle Arbeit mehr erforderlich ist
Entfernen der Säule und Wechseln des Lösungsmittels. Diese Automatisierung erhöht die Effizienz und den Komfort des Analyseprozesses erheblich.

Oligo(dT) 12-18-Primer
Der Oligo(dT) 12-18-Primer (Thermos Fisher Scientific, MA) wurde verwendet, um die HPLC-Methode für die Oligonukleotidanalyse zu überprüfen.
Die Trennung dieser Oligo(dT) 12-18-Primer wurde unter Verwendung einer Ionenpaar-Umkehrphasen-HPLC-Methode mit einer Interchim Uptisphere Strategy 5 μm C18HQ-Säule 250 x 4.6 mm durchgeführt. Für alle Analysen wurde ein 10-μl-Aliquot injiziert und die Säulentemperatur wurde bei 30 °C gehalten. Die Zusammensetzung der mobilen Phase A bestand aus 100 mM TEAA in Wasser, während die mobile Phase B Acetonitril ist. Und die Durchflussrate beträgt 1 ml/min.
Die HPLC-Analyse verlief wie folgt: Nach Injektion der Probe wurde die mobile Phase B für 10 Minute auf 1 % eingestellt. Anschließend wurde sie über 15 Minuten linear auf 24 % erhöht. Bei 25.1 Minuten stieg er auf 95 % und wurde 2.4 Minuten lang auf diesem Niveau gehalten, um die Säule zu reinigen. Anschließend wurde er nach 27.6 Minuten auf 10 % reduziert und zur Säulenäquilibrierung 2.4 Minuten lang beibehalten.
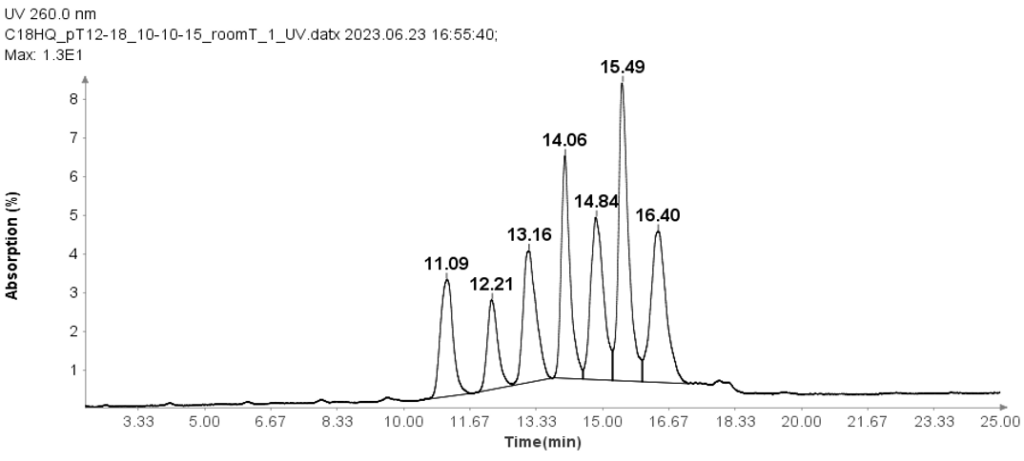
Abbildung 1 zeigt, dass die HPLC-Methode die sieben Oligo(dT) 12 bis 18-Primer effektiv trennt.
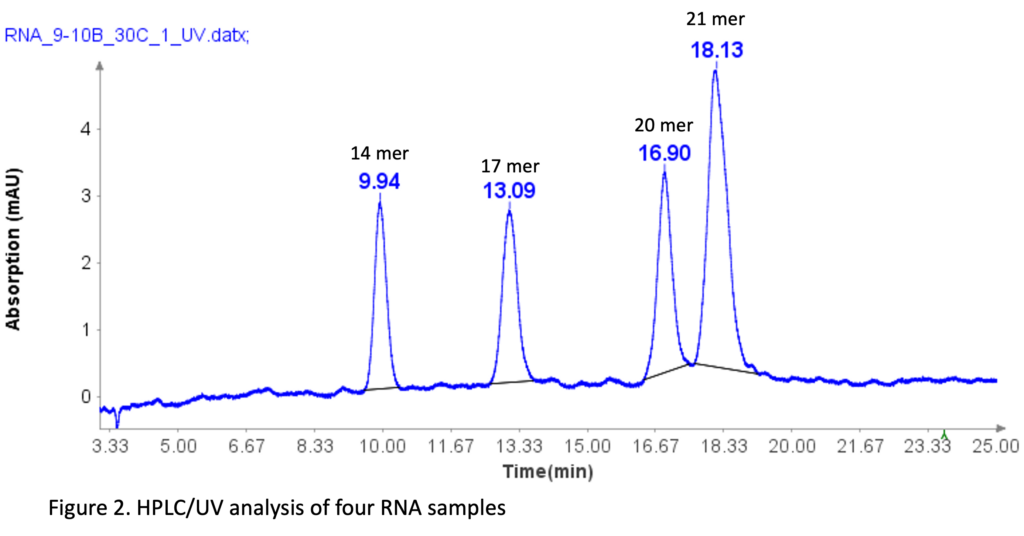
RNA-Standard mit 4 Komponenten
Die RNA-Oligonukleotidmischung (Aglient Technologies, CA) wurde durch zehnfache Verdünnung mit entionisiertem Wasser vor der HPLC-Analyse hergestellt. Die Sequenzen von vier RNA-Standards sind wie folgt: 10-mer (CACUGAAUACCAAU), 14-mer (UCACACUGAAUACCAAU), 17-mer (UCAUCACACUGAAUACCAAU) und 20-mer (GUCUCAUCACACUGAAUACCAAU).
Die Trennung dieser RNA-Proben wurde mit geringfügigen Modifikationen mit einer ähnlichen HPLC-Methode wie für Oligo(dT)12-18-Primer durchgeführt.
Die HPLC-Analyse verlief wie folgt: Nach Injektion der Probe wurde die mobile Phase B für 9 Minute auf 1 % eingestellt. Anschließend wurde sie über 10 Minuten linear auf 24 % erhöht. Bei 25.1 Minuten stieg er auf 95 % und wurde 2.4 Minuten lang auf diesem Niveau gehalten, um die Säule zu reinigen. Anschließend wurde er nach 27.6 Minuten auf 9 % reduziert und zur Säulenäquilibrierung 2.4 Minuten lang beibehalten.
Abbildung 2 zeigt, dass die HPLC-Methode die vier RNA-Proben effektiv trennt, selbst bei einem 1-mer-Unterschied zwischen den 20-mer- und 21-mer-RNA-Proben. Diese Grundlinientrennung für das 20-mer und 21-mer ist für die Analyse synthetischer Oligonukleotide von entscheidender Bedeutung, da die meisten Verunreinigungen während der Synthese typischerweise N=1-mer oder N+1-mer sind.[2].
ssDNA-Proben
Drei einzelsträngige DNA-Proben (ssDNA) mit 17-mer (GTCAGCAAGGACATCGT), 18-mer (CATTTGAGTAGCCAACGC) und 19-mer (GGACACTTTCATGCGAGTT) wurden ebenfalls mit der gegenüber RNA-Proben modifizierten HPLC-Methode getestet.
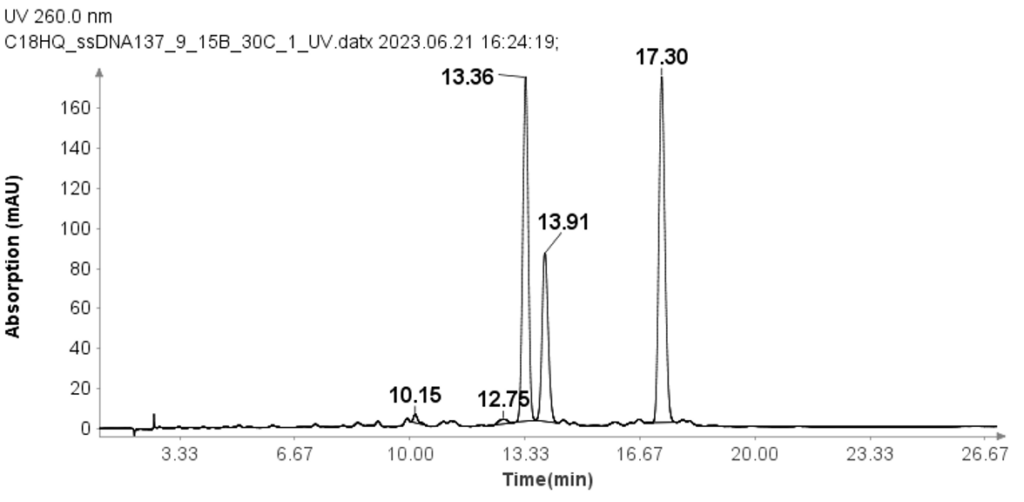
Die Konzentration jeder ssDNA betrug 30 μM und 10 μL-Aliquots wurden zur Analyse auf die Säule geladen. Die HPLC-Analyse wurde mit dem folgenden Gradienten durchgeführt: Nach der Probeninjektion wurde die mobile Phase B (MPB) 9 Minute lang auf 1 % eingestellt und dann über 15 Minuten linear auf 24 % erhöht. Bei 25.1 Minuten stieg er auf 95 % und wurde 2.4 Minuten lang auf diesem Niveau gehalten, um die Säule zu reinigen. Nach 27.6 Minuten war der MPB auf 9 % reduziert und dieser Wert wurde zur Säulenäquilibrierung 2.4 Minuten lang beibehalten. Die Flussrate für die Analyse wurde auf 1.5 ml/min eingestellt. Trotz der größeren Änderung des Lösungsmittels B pro Minute im Vergleich zu den RNA-Proben zeigt Abbildung 3, dass die Methode die drei ssDNA-Proben effektiv mit guter Grundlinienauflösung trennt.
Reinheitsanalyse einer ssDNA-Probe
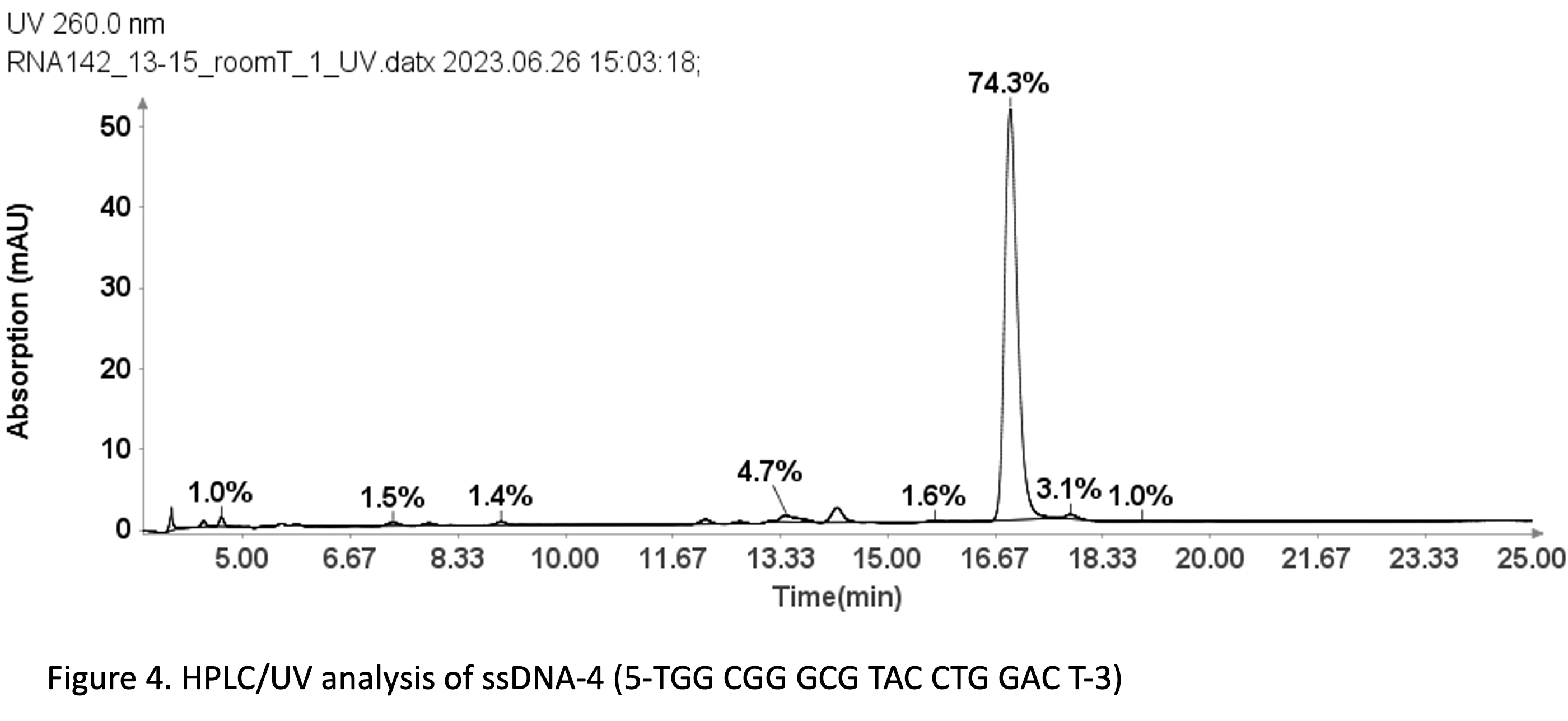
Mit der gleichen Methode, die für ssDNA-Proben verwendet wird (siehe Abbildung 3), wurde sie auch für die Reinheitsanalyse einer ssDNA-Probe verwendet: 19 mer (5'-TGGCGGGCGTACCTGGACT-3').
Abbildung 4 zeigt, dass die 19-mer-ssDNA 4 eine UV-Reinheit von 74.3 % bei 260 nm aufweist, die mit der Advion Data Express-Software bestimmt wurde.
MS-Analyse der ssDNA-Probe, die in der F.5-Reinheitsanalyse verwendet wird
Die HPLC/MS-Analyse der Oligonukleotide wurde mit einem Advion AVANT durchgeführt® HPLC-System gekoppelt mit einem Advion ExPresseIon® CMS-L. Für die MS-Analyse wurde die Interchim Uptisphere Strategy 2.6 μm C18-HQ-Säule mit den Abmessungen 50 x 2.1 mm und einer Flussrate von 0.2 ml/min verwendet. Die Säulentemperatur wurde auf 55°C eingestellt.
Im Vergleich zur Verwendung von TEAA für die Massenanalyse von Oligonukleotiden bieten die Ionenpaarreagenzien, die TEA und HFIP kombinieren, eine deutlich verbesserte Leistung. Daher konzentriert sich dieser Anwendungshinweis auf den Einsatz von TEA- und HFIP-Ionenpaarreagenzien für die HPLC/MS-Analyse von Oligonukleotiden.
Die mobile Phase bestand aus 15 mM TEA und 10 mM HFIP in Wasser als mobile Phase A und Methanol als mobile Phase B. Die gesamte HPLC-Laufzeit betrug 25 Minuten, beginnend mit 5 % Lösungsmittel B für 1 Minute.
Der B-Prozentsatz wurde dann innerhalb von 6 Minuten auf 14 % erhöht, gefolgt von einem Anstieg auf 95 % nach 15.1 Minuten, der 2.9 Minuten lang beibehalten wurde, um die interessierenden Verbindungen zu eluieren. Anschließend wurde der % B-Gehalt auf 5 % reduziert und 6.9 Minuten lang auf diesem Niveau gehalten, um die Säule vor der nächsten Analyse ins Gleichgewicht zu bringen.
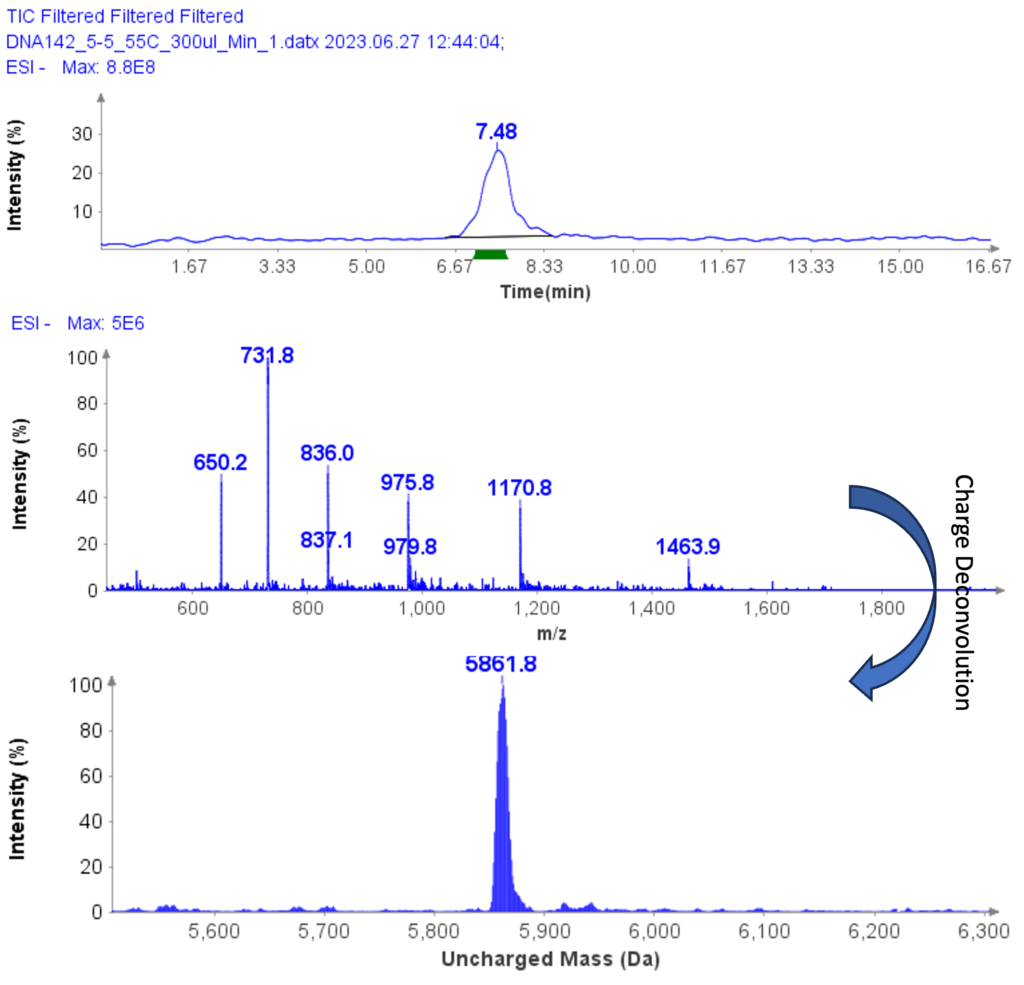
Die MS-Analyse wurde im negativen ESI-Modus durchgeführt, wobei der MS-Scanbereich auf 500 bis 2000 Da eingestellt war. Abbildung 5b zeigt die MS-Spektren von ssDNA-4 und zeigt eine geladene Hülle mit Peaks bei m/z 1463.9 (4-), 1170.8 (5-), (975.8 (6-), 936.0 (7-), 731.8 (8-). ) und 650.2 (9-). Durch Ladungsentfaltung in Data Express wurde die ungeladene Masse für die ssDNA-Probe zu 5861.8 Da bestimmt, was dem theoretischen Wert von 5860.8 Da sehr nahe kommt.
MS-Analyse einer weiteren Beispielprobe
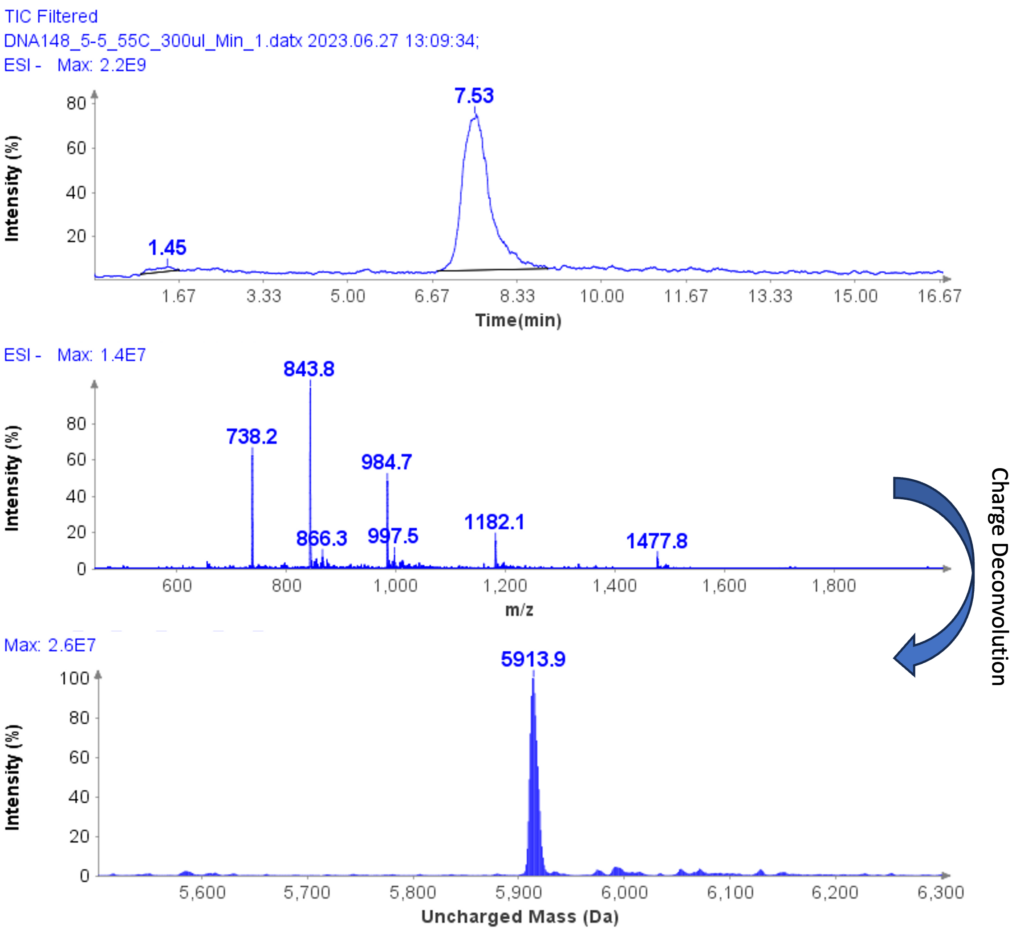
Die MS-Spektren von ssDNA-5 (5'-GGG-TGG-CAT-TATGCT-GAG-T-3') sind in Abbildung 6 dargestellt und zeigen eine geladene Hülle mit Peaks bei m/z 1477.8(4-), 1182.1( 5-), 984.7(6-), 843.8(7-) und 738.2(8-). Durch Ladungsentfaltung wurde die ungeladene Masse für ssDNA-5 zu 5913.9 bestimmt, was gut mit dem theoretischen Wert von 5914.9 übereinstimmt.
Fazit
Die Verwendung einer C5HQ-Säule mit einer Partikelgröße von 18 μm in Verbindung mit dem Ionenpaarungsreagenz TEAA (Triethylammoniumacetat) hat sich als geeignete Lösung für die Oligonukleotid-HPLC-Analyse erwiesen.
Für die MS-Analyse von Oligonukleotiden kann dieselbe C18HQ-Säule mit HFIP (Hexafluorisopropanol) und TEA (Triethylamin) als Ionenpaarungsreagenz in Verbindung mit einem AVANT verwendet werden® HPLC-UV/CMS-System. Diese Methode liefert nachweislich zusätzliche genaue Massenmessungen von Oligonukleotiden.
Insgesamt wurde die Interchim C18HQ-Säule und das entsprechende Ionenpaarungsreagenz in Kombination mit AVANT verwendet® HPLC-UV- und -CMS-Systeme können eine zuverlässige Lösung für die Reinheitsanalyse und Charakterisierung von Oligonukleotiden bieten.
Referenzen
[1].Roberts, TC, Langer, R. & Wood, MJA Fortschritte bei der Oligonukleotid-Arzneimittelabgabe. Nat Rev Drug Discov 2020, 19, 673–694
[2].Martina C. et.al. Oligonukleotide: Aktuelle Trends und innovative Anwendungen in der Synthese, Charakterisierung und Reinigung, Biotechnology J. 2020, 1900226

