冬季等离子会议
使用 Advion Interchim Scientific 进行寡核苷酸定性分析® 高效液相色谱-紫外/质谱系统

仪表
质谱: 前任expression® 紧凑型质谱仪(CMS)
HPLC:前卫®
引言
寡核苷酸由于其独特的优势而在生物制药领域受到广泛关注。
调节基因或蛋白质表达的能力。 随着几种基于寡核苷酸的药物获得批准或进入临床试验,他们的临床成功是显而易见的。[1] 这些药物包括反义寡核苷酸、小干扰 RNA (siRNA) 疗法和基于 mRNA 的疫苗,新冠肺炎 (COVID-19) 疫苗的成功开发就是例证。 这些成就激发了人们对寡核苷酸研究和开发的进一步兴趣和投资。
固相合成是生产寡核苷酸序列的常用方法。 原材料通常通过各种技术进行纯化,例如脱盐、超滤、固相萃取 (SPE)、高效液相色谱 (HPLC) 或制备型液相色谱 (prepLC),具体取决于所需的纯度水平。 离子对 HPLC 或 prepLC 方法通常是首选,因为与其他技术相比,它们可提供更高的纯度。
本应用说明旨在演示多种寡核苷酸样品的 HPLC/UV 分析,并利用 HPLC/CMS 分析确定其分子量。
付款方式
HPLC-UV/CMS系统
借助四元泵和色谱柱选择阀,在不同缓冲液和色谱柱之间进行各种分析的切换过程变得非常简单,无需手动操作
拆下色谱柱并更换溶剂。 这种自动化极大地提高了分析过程的效率和便利性。

Oligo(dT) 12-18 引物
使用 Oligo(dT) 12-18 引物(Thermos Fisher Scientific,MA)检查寡核苷酸分析的 HPLC 方法。
这些 Oligo(dT) 12-18 引物的分离是使用离子对反相 HPLC 方法和 Interchim Uptisphere Strategy 5 μm C18HQ 色谱柱 250 x 4.6 mm 进行的。 所有分析均注入 10 μL 等分试样,柱温保持在 30°C。 流动相 A 的组成为 100 mM TEAA 水溶液,而流动相 B 为乙腈。 流速为1ml/min。
HPLC 分析进行如下:注入样品后,将流动相 B 设置为 10%,持续 1 分钟。 然后在 15 分钟内线性增加到 24%。 在 25.1 分钟时,它增加到 95%,并在此水平保持 2.4 分钟以清洗色谱柱。 随后,在 27.6 分钟时,其减少至 10%,并维持 2.4 分钟以进行柱平衡。
图 1 说明 HPLC 方法有效分离了 12 个 Oligo(dT) 18 至 XNUMX 引物。
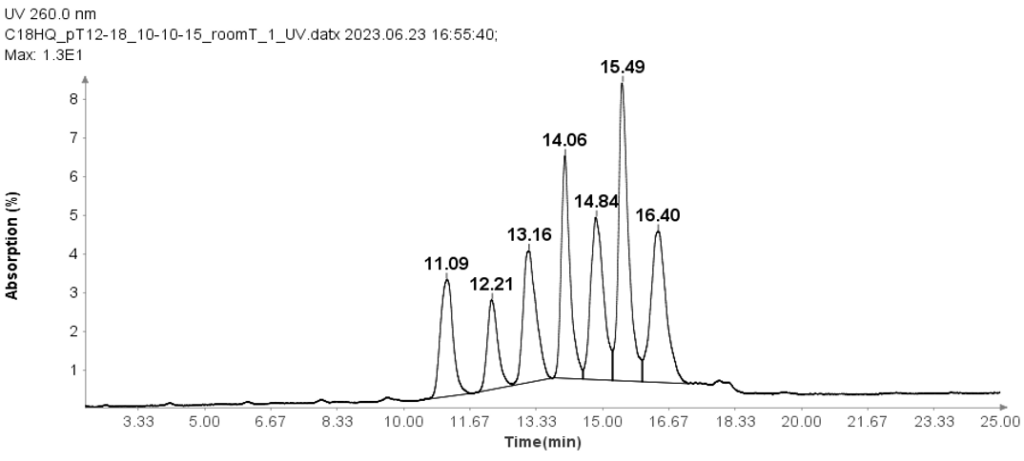
含 4 种成分的 RNA 标准品
RNA 寡核苷酸混合物(Aglient Technologies,CA)在 HPLC 分析之前用去离子水稀释 10 倍来制备。 四种RNA标准品的序列如下:14 mer(CACUGAAUACCAAU)、17 mer(UCACACUGAAUACCAAU)、20 mer(UCAUCACACUGAAUACCAAU)和21 mer(GUCUCAUCACACUGAAUACCAAU)。
这些 RNA 样品的分离使用与oligo(dT)12-18 引物类似的 HPLC 方法进行,但略有修改。
HPLC 分析进行如下:注入样品后,将流动相 B 设置为 9%,持续 1 分钟。 然后在 10 分钟内线性增加到 24%。 在 25.1 分钟时,它增加到 95%,并在此水平保持 2.4 分钟以清洗色谱柱。 随后,在 27.6 分钟时,其减少至 9%,并维持 2.4 分钟以进行柱平衡。
图 2 说明 HPLC 方法可以有效分离四种 RNA 样品,即使 1 聚体和 20 聚体 RNA 样品之间存在 21 聚体差异。 20 聚体和 21 聚体的基线分离对于分析合成寡核苷酸至关重要,因为合成过程中的大多数杂质通常为 N=1 聚体或 N+1 聚体。[2]
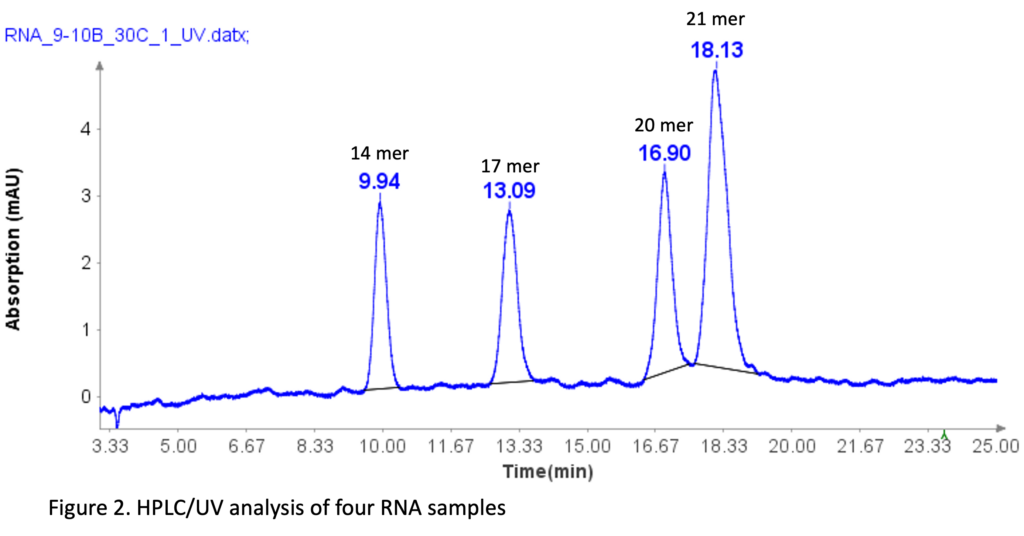
单链DNA样本
还使用用于 RNA 样品的改进 HPLC 方法测试了具有 17 mer (GTCAGCAAGGACATCGT)、18 mer(CATTTGAGTAGCCAACGC) 和 19 mer (GGACACTTTCATGCGAGTT) 的三个单链 DNA 样品 (ssDNA)。
每个 ssDNA 的浓度为 30 μM,将 10 μL 等份上样到柱上进行分析。 使用以下梯度进行 HPLC 分析:样品注射后,流动相 B (MPB) 设置为 9%,持续 1 分钟,然后在 15 分钟内线性增加至 24%。 在 25.1 分钟时,它增加到 95%,并在此水平保持 2.4 分钟以清洗色谱柱。 27.6 分钟时,MPB 降至 9%,并维持该水平 2.4 分钟以进行柱平衡。 分析的流速设置为1.5ml/min。 尽管与 RNA 样品相比,每分钟溶剂 B 的变化更大,但图 3 表明该方法以良好的基线分辨率有效分离了三个 ssDNA 样品。
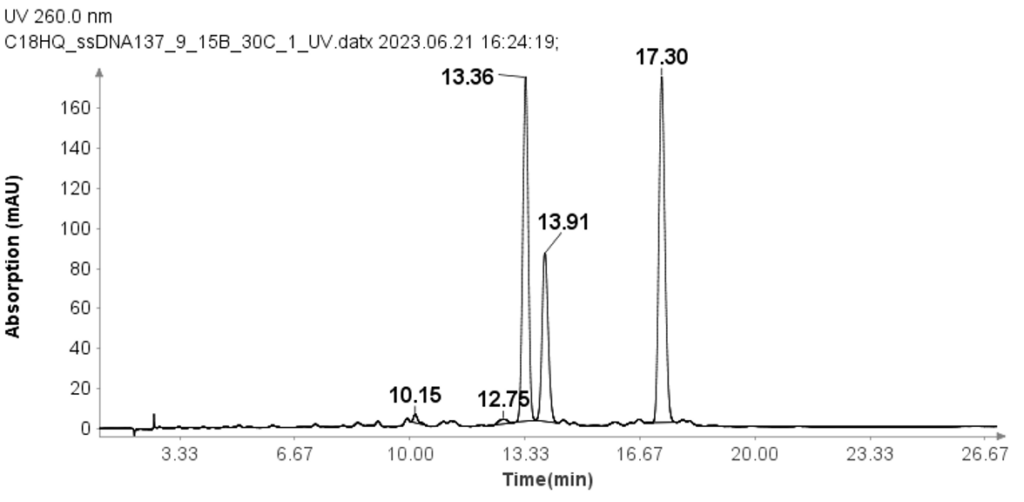
单链 DNA 样品的纯度分析
采用与图 3 所示的 ssDNA 样品相同的方法,也可用于 ssDNA 样品的纯度分析:19 mer (5'-TGGCGGGCGTACCTGGACT-3')。
图 4 显示,使用 Advion Data Express 软件测定的 19 聚体 ssDNA 4 在 74.3 nm 处的 UV 纯度为 260%。
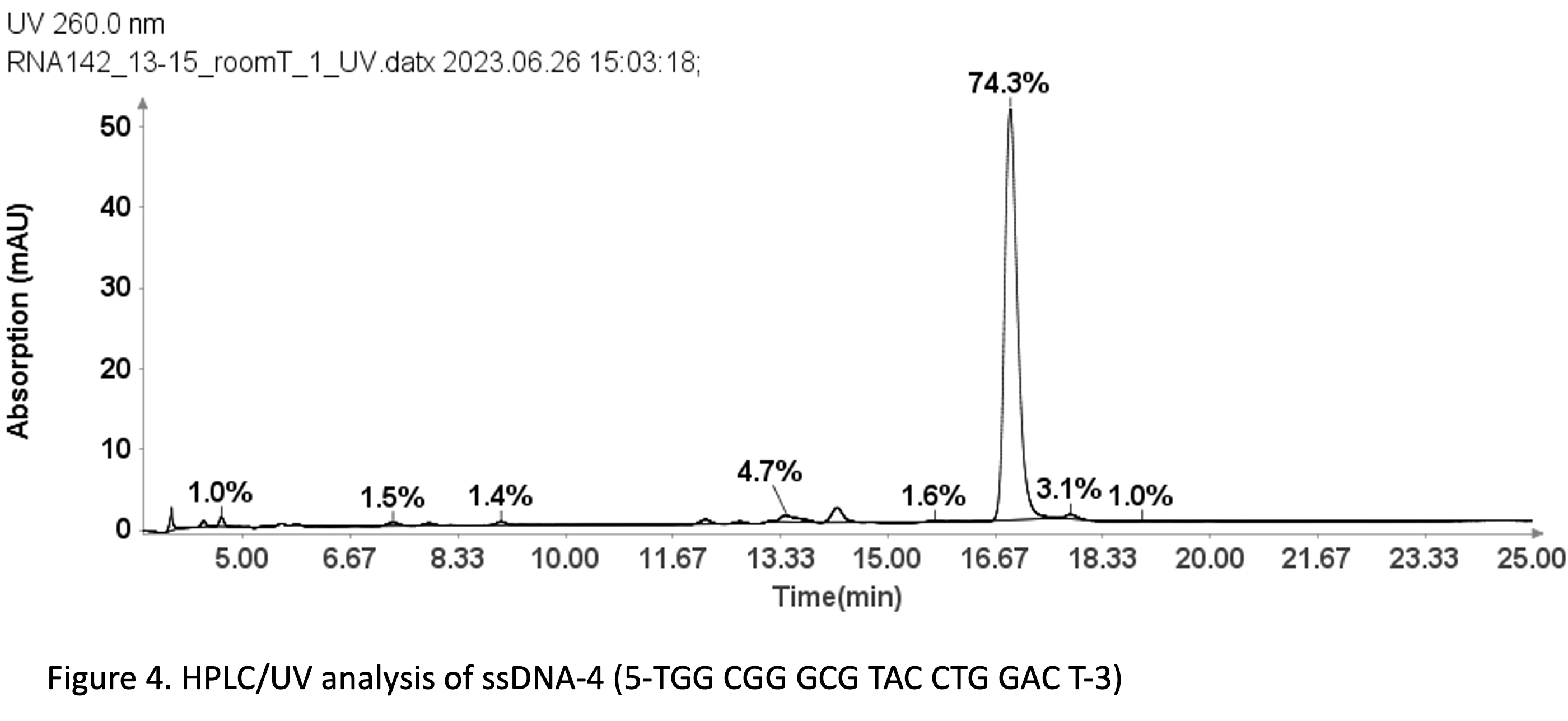
F.5 纯度分析中使用的 ssDNA 样品的 MS 分析
使用 Advion AVANT 进行寡核苷酸的 HPLC/MS 分析® 与 Advion Ex 结合的 HPLC 系统expression® CMS-L。 对于 MS 分析,使用尺寸为 2.6 x 18 mm 的 Interchim Uptisphere Strategy 50 μm C2.1-HQ 色谱柱,流速为 0.2 ml/min。 柱温设定为55℃。
与使用 TEAA 进行寡核苷酸质量分析相比,结合 TEA 和 HFIP 的离子对试剂可显着提高性能。 因此,本应用笔记将重点介绍如何使用 TEA 和 HFIP 离子对试剂对寡核苷酸进行 HPLC/MS 分析。
流动相由 15 mM TEA 和 10 mM HFIP 水溶液(作为流动相 A)和甲醇(作为流动相 B)组成。总 HPLC 运行时间为 25 分钟,从 5% 溶剂 B 开始 1 分钟。
然后 B 的百分比在 6 分钟内增加至 14%,随后在 95 分钟增加至 15.1%,并保持 2.9 分钟以洗脱感兴趣的化合物。 随后,将 % B 降低至 5%,并在此水平保持 6.9 分钟,以便在下一次分析之前平衡色谱柱。
MS 分析在负 ESI 模式下进行,MS 扫描范围设置为 500 至 2000 Da。 图 5b 显示了 ssDNA-4 的 MS 谱图,显示带电包络,峰位于 m/z 1463.9 (4-)、1170.8 (5-)、(975.8 (6-)、936.0 (7-)、731.8 (8-) ) 和 650.2 (9-)。通过 Data Express 中的电荷解卷积,确定 ssDNA 样品的不带电质量为 5861.8 Da,这与理论值 5860.8 Da 非常吻合。
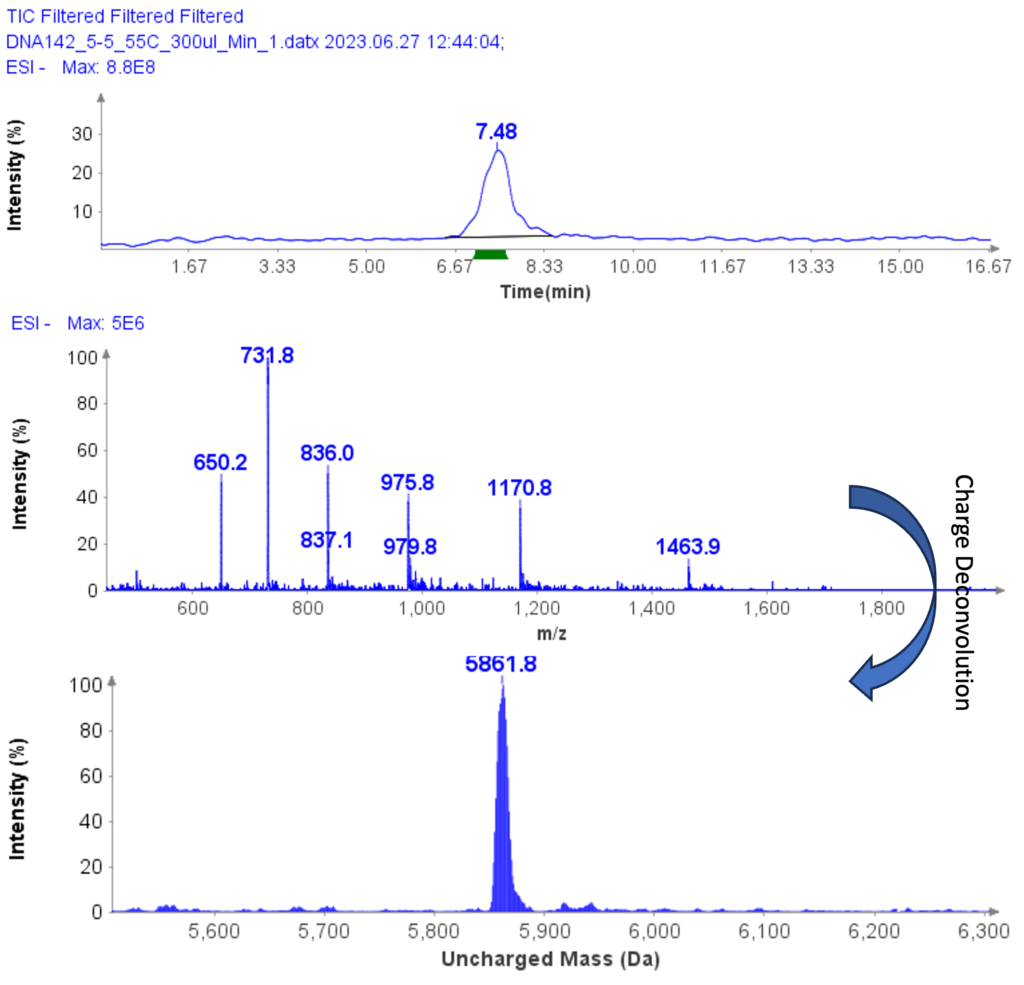
另一个示例样品的 MS 分析
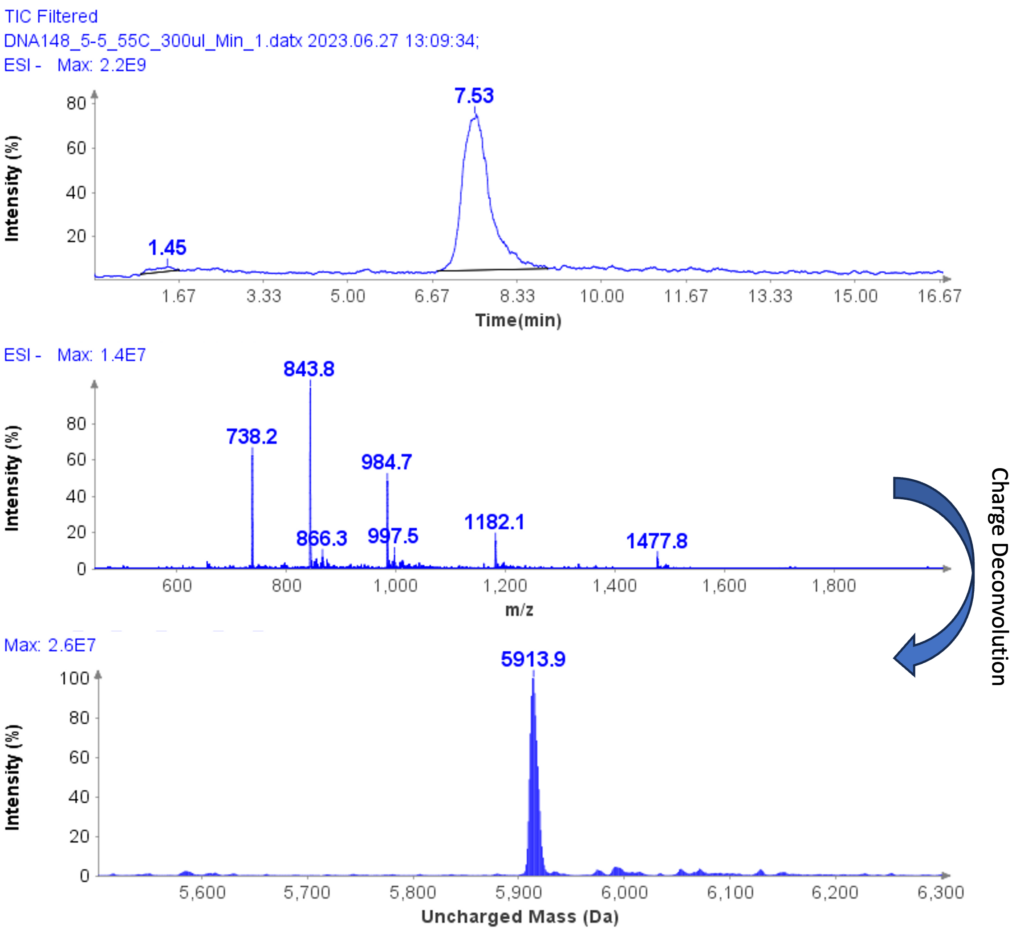
ssDNA-5 (5'-GGG-TGG-CAT-TATGCT-GAG-T-3') 的 MS 谱如图 6 所示,显示带电包络,峰位于 m/z 1477.8(4-)、1182.1( 5-)、984.7(6-)、843.8(7-) 和 738.2(8-)。 通过电荷解卷积,确定 ssDNA-5 的不带电质量为 5913.9,这与理论值 5914.9 非常一致。
结语
事实证明,使用 5 μm 粒径的 C18HQ 色谱柱与 TEAA(醋酸三乙铵)离子对试剂结合是寡核苷酸 HPLC 分析的合适解决方案。
对于寡核苷酸的 MS 分析,可以使用相同的 C18HQ 色谱柱,将 HFIP(六氟异丙醇)和 TEA(三乙胺)作为离子对试剂与 AVANT 结合使用® HPLC-UV/CMS 系统。 该方法已被证明可以对寡核苷酸进行额外的精确质量测量。
总体而言,将 Interchim C18HQ 色谱柱和适当的离子对试剂与 AVANT 结合使用® HPLC-UV和-CMS系统可以为寡核苷酸的纯度分析和表征提供可靠的解决方案。
案例
[1]Roberts, TC、Langer, R. 和 Wood, MJA 寡核苷酸药物输送方面的进展。 自然修订药物发现 2020, 19, 673–694
[2]玛蒂娜·C.等人寡核苷酸:合成、表征和纯化的当前趋势和创新应用,Biotechnology J. 2020, 1900226
SWRM:西南区域会议
药学360
OHSU 化学生物学与生理学 2023
美国国立卫生研究院秋季研究节 2023
EAS 2023:东方分析研讨会
2023 年上海国际汽车展览会
使用 puriFlash® 5.250 PrepLC 和 ex 从复杂混合物中纯化生物活性肽expression® CMS 探测器
仪表
质谱: exexpression® CMS
闪光灯: puriFlash® 5.250 制备液相色谱
HPLC: AVANT®
作者
郝长通
Advion Interchim 科学
引言
近年来,生物制药公司越来越多地采用基于肽/蛋白质的药物,因为与传统的小分子药物相比,它们具有增强的特异性和选择性。 然而,药物发现过程中肽/蛋白质的纯化对于确保最终产品的安全性和有效性至关重要。 生物活性目标化合物达到尽可能高的纯度对于最大限度地降低毒性风险和遵守监管标准至关重要。[1,2]
乳清分离蛋白是奶酪生产的副产品,含有多种糖巨肽和两种重要的生物活性肽,即分子量 (MW) 为 6757 Da 的酪蛋白巨肽 A (CMPa) 和分子量 (MW) 为 6787 Da 的酪蛋白巨肽 B (CMPb) 。 提取和纯化单个成分,例如酪蛋白
巨肽对于研究其生物活性至关重要。[3]
在本应用说明中,我们以乳清分离蛋白和两种酪蛋白巨肽为例,演示使用 puriFlash 组成的系统分离和纯化生物活性成分® 5.250 prepLC 在线耦合到 exexpression® CMS 检测器。 与 UV 或 ELSD 等传统检测器相比,这种组合提供了更高的选择性和灵敏度,传统检测器可能无法有效地响应生物活性目标肽和蛋白质。

Advion Interchim 科学
puriFlash® 5.250

Advion Interchim 科学
exexpression® CMS
付款方式
乳清分离蛋白的制备
• 本申请中使用的酪蛋白巨肽分离程序基于 Tadao Saito 的工作[4] 有一些修改。
• 将从当地杂货店购买的 50 g 乳清分离蛋白样品与 500 mL 70% 水和 30% 甲醇 (v/v) 的溶剂混合物混合。 将混合物在70℃下超声处理90分钟,然后减压过滤。
·使用旋转蒸发器在300℃减压下除去甲醇,将所得滤液浓缩至体积40mL。 然后将其在 4°C 下保存一小时。 随后,将等体积的冷乙醇添加到溶液中,并将混合物涡旋5分钟,然后在4°C下再保存4小时。
·使用0.5μm过滤器在减压下过滤混合物。 然后使用旋转蒸发器在减压下将最终滤液浓缩至体积50mL。
• 将 100 µL 等份浓缩提取物与 900 µL 去离子 (DI) 混合
用于分析型 HPLC/MS 分析的水。
• 剩余的滤液用于使用 puriFlash 进行肽纯化® 5.250 PrepLC 系统与 ex 耦合expression® CMS 检测器。
表1: 分析 HPLC/MS 方法设置
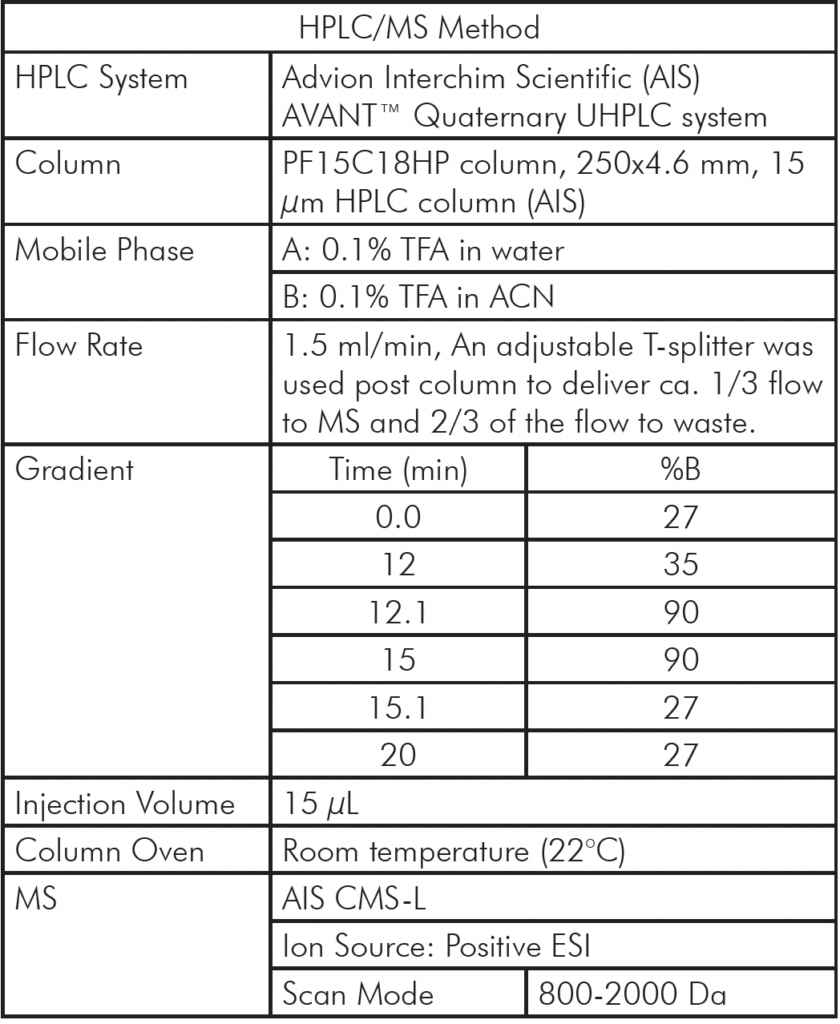
分析 HPLC/MS 方法设置
首先使用 AVANT 分析乳清分离蛋白的液体提取物® HPLC/CMS 系统和针对所用 4.6 mm 色谱柱开发的色谱分离方法(表 1)。
图 1a 显示了液体提取物的 HPLC/MS 色谱图。 6.44 分钟处峰的平均 MS 谱表明该化合物是多电荷肽,在 m / z 755.2、849.4、970.6、1132.1 和 1358.6(图 1b)形成电荷分布。
通过软件电荷反卷积,确定肽的不带电荷质量为 6787.4 Da,表明酪蛋白巨肽 B(CMPb,理论质量为 6787 Da)(图 1c)。

Advion Interchim 科学
AVANT® (U)HPLC
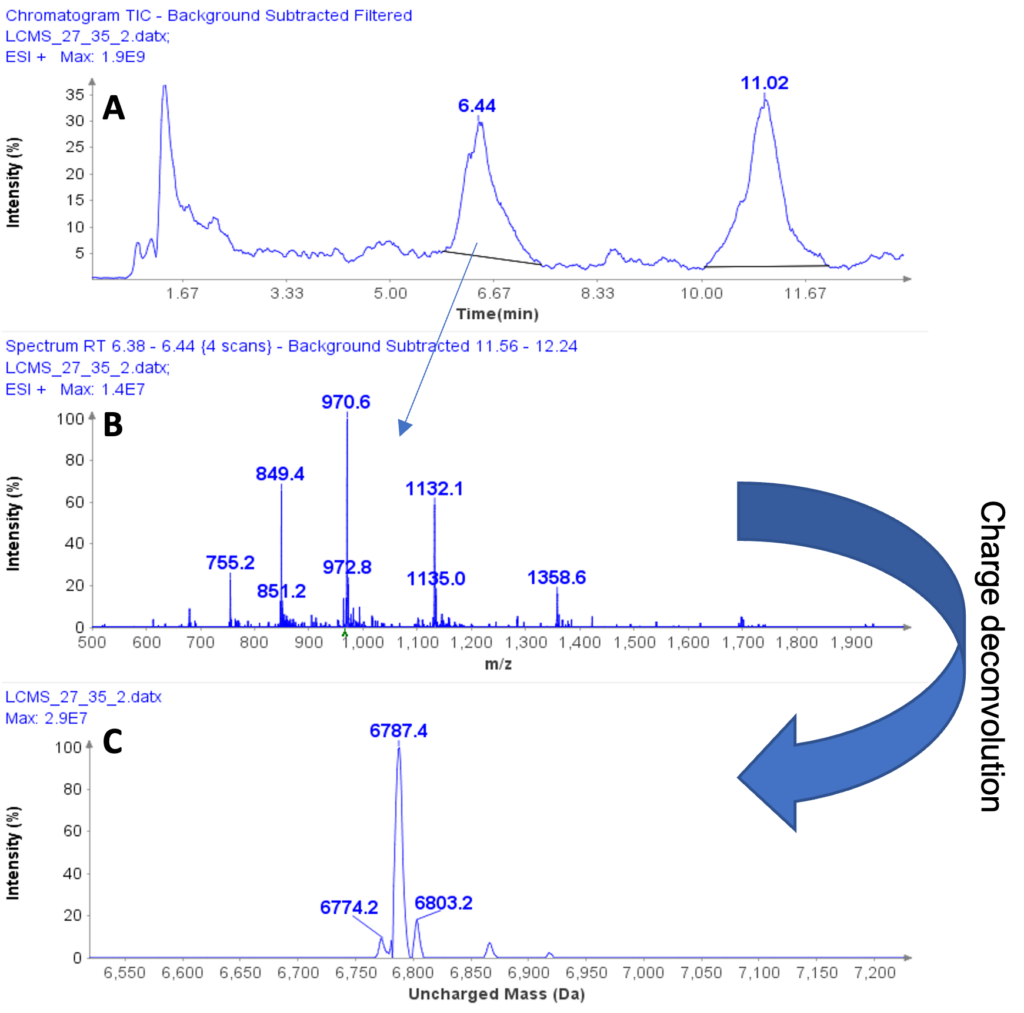
图1: (a) 乳清蛋白分离物液体提取物的 HPLC/MS 色谱图,(b) 室温 6.44 分钟处峰的平均 MS 谱图,(c) 室温 6.44 分钟处肽洗脱峰的解卷积、不带电质量。
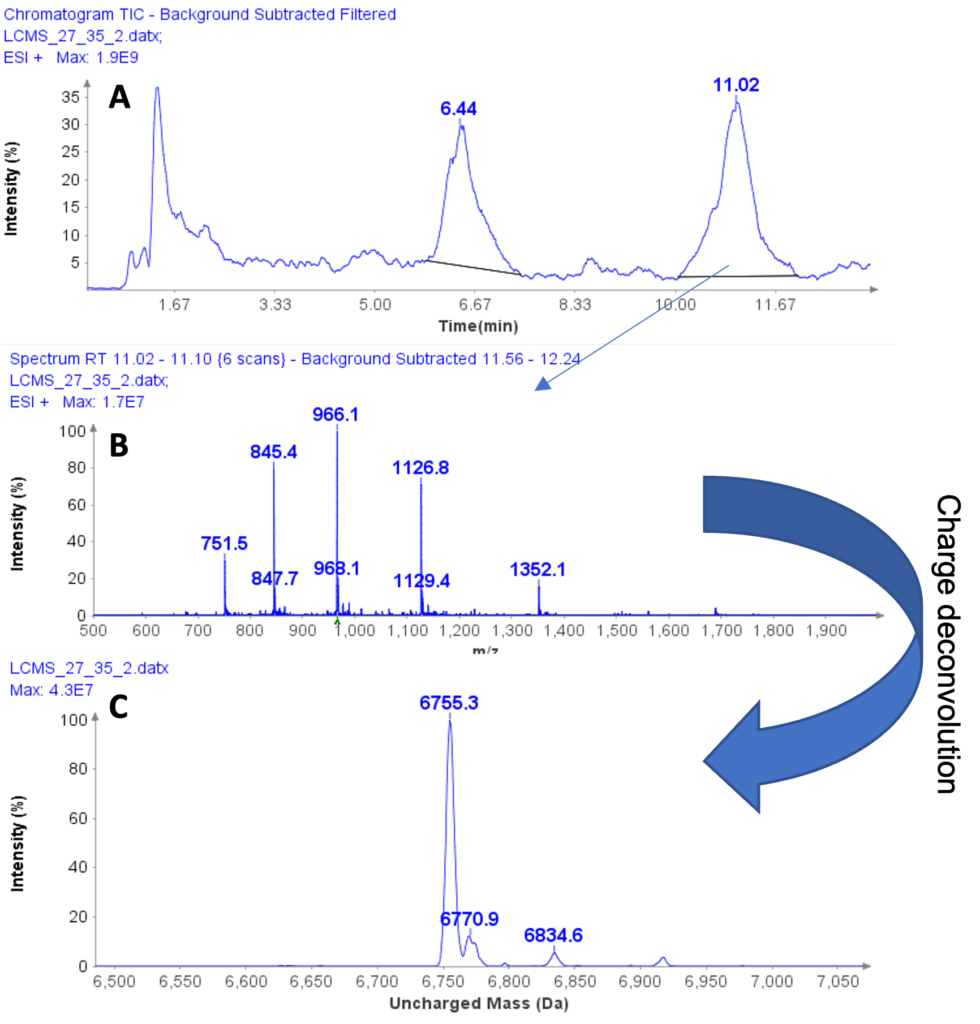
图2: (a) 乳清蛋白分离物液体提取物的 HPLC/MS 色谱图,(b) 室温 11.02 分钟时峰的平均 MS 谱图,(c) 室温 11.02 分钟时洗脱的肽的解卷积、不带电质量。
从 11.02 分钟洗脱峰获得的平均 MS 谱表明,该化合物也是一种多电荷肽,质量为 m/z 751.5、845.4、966.1、1126.8 和 1352.1(图 2b),形成其电荷分布。
同样,电荷解卷积确定该肽的不带电质量为 6755.3 Da,表明酪蛋白巨肽 A 变体 CMPa 的理论质量为 6755 Da(图 2c)。

Advion Interchim 科学
puriFlash® 5.250,MS 分离器和前expression® CMS
PrepLC/MS 色谱法
下一步,将分析分离方法转换为更大的制备规模,从 4.6 mm 柱内径改为 30 mm 柱内径,并进一步优化 puriFlash 上两种 CMP(酪蛋白糖巨肽)的纯化® 5.250 PrepLC/Flash 系统与 ex 在线耦合expression® CMS 检测器。
乳清分离蛋白的 PrepLC-UV/MS 色谱图如图 3 所示,参数如表 2 所示。
馏分收集是根据 MS 信号触发的,之所以选择 MS 信号是因为它具有更高的选择性和灵敏度。 970-971 Da 的 XIC 用于检测 CMPb,965-966 Da 的 XIC 用于检测 CMPa。
使用旋转蒸发器在负压下除去级分11-17和级分18-22的组合中的有机溶剂,并且剩余的水性溶液
使用 LABCONCO Freezone 2.5L(-50℃)冻干机干燥溶液,得到每份 10 mg 的干燥收集物,然后将其溶解在 10 ml 去离子水中用于后续 HPLC/UV/MS 分析。 纯度分析结果如图4和图6所示。
表2: PrepLC/MS 方法设置
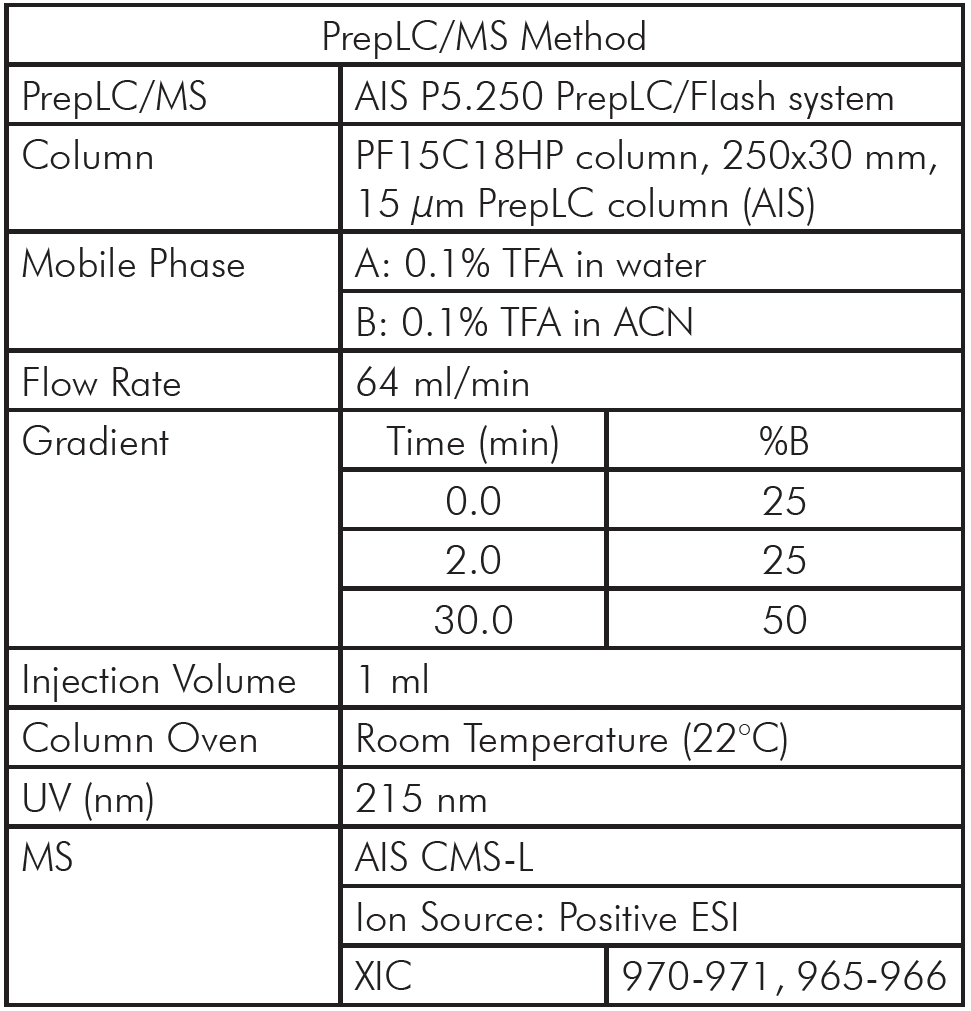
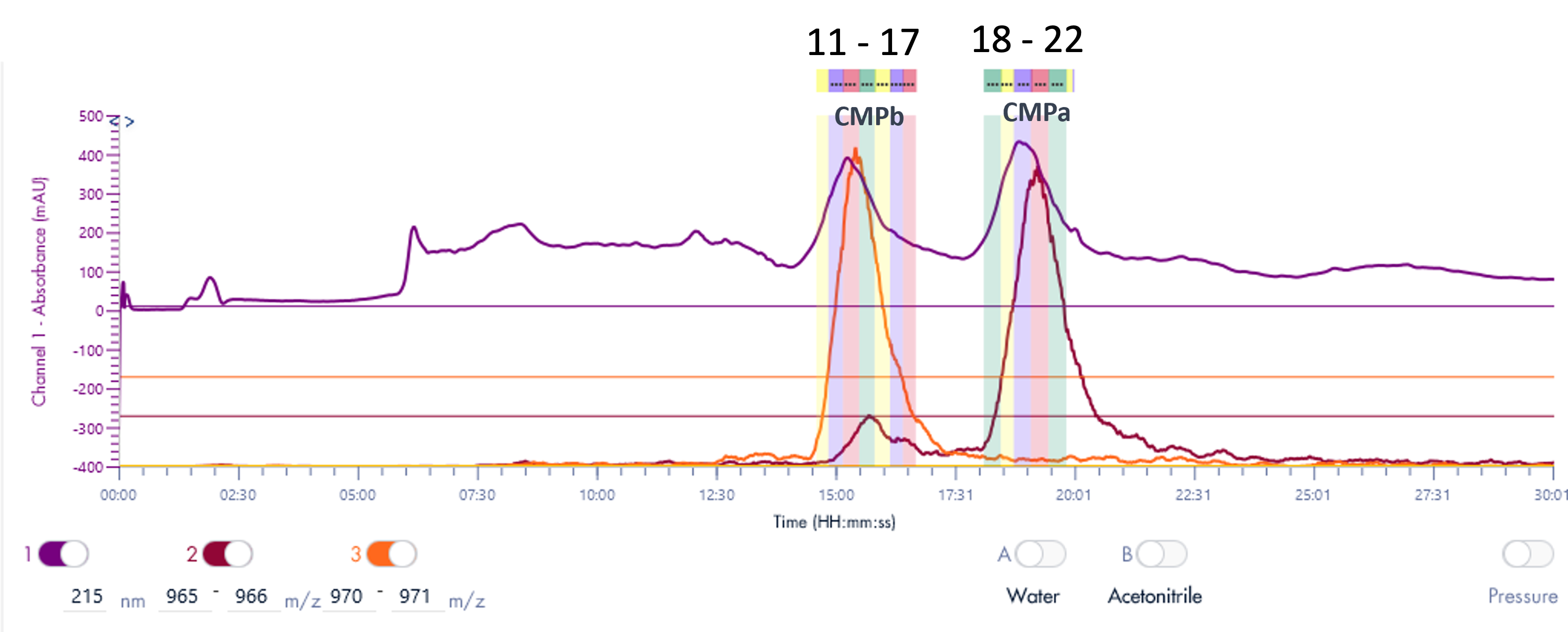
图3: 两种乳清分离蛋白的 PrepLC-UV/MS 色谱图
功能验证
CMPb 的纯度分析
合并级分 11 至 17 中 CMPb 的纯度分析如图 4 所示。MS 分析显示检测到四种主要离子,m/z 分别为 970.8、1132.3、1358.6 和 1968.2(图 4b)。
根据图 4b 的平均质谱,确定 5.94 分钟处峰的不带电质量为 6788.4(CMPb,图 4c)。 然而,MS 分析还可以检测 6758.3、6773.5、6804.8 和 6868.4 Da 处的四种微量成分。
获得的 CMPb 的 UV 纯度为 86.7%(图 4d),但是根据额外的 MS 数据,化合物纯度实际上低于该值(估计为 80%)。
根据分析运行的 UV 分析,测得合并级分 18 至 22 中的 CMPa 为 94.7%(图 5a)。
解卷积不带电质量分析显示 CMPa 的预期主要质量为 6756.2(图 5b),以及 6774.6 处的一个次要成分(CMPa 的氧化形式)。
该示例再次显示了 MS 检测肽和蛋白质等生物活性化合物的价值,以及与 UV 相比 MS 检测具有更好的特异性。
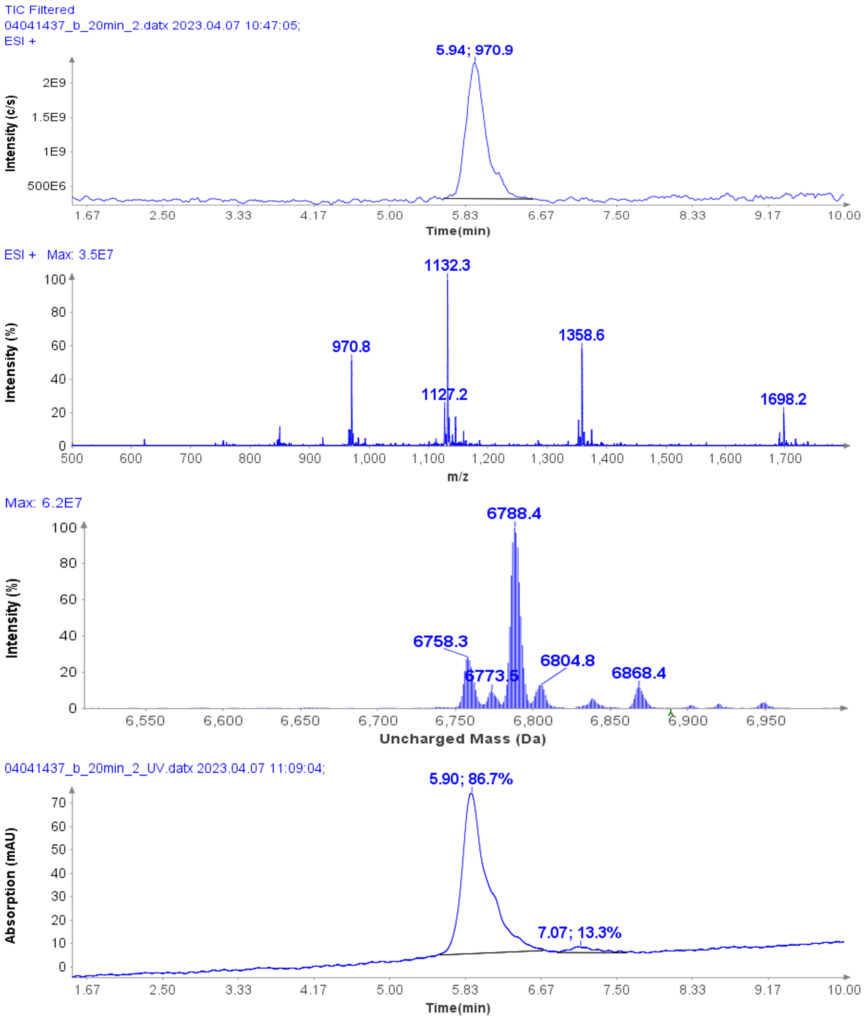
图4: (a) 11-17 合并馏分的 HPLC-MS 色谱图,(b) 在 RT 5.94 分钟时洗脱的峰的平均 MS 谱图,(c) (b) 中的不带电质量,(d) 合并馏分的 HPLCUV 色谱图11-17。
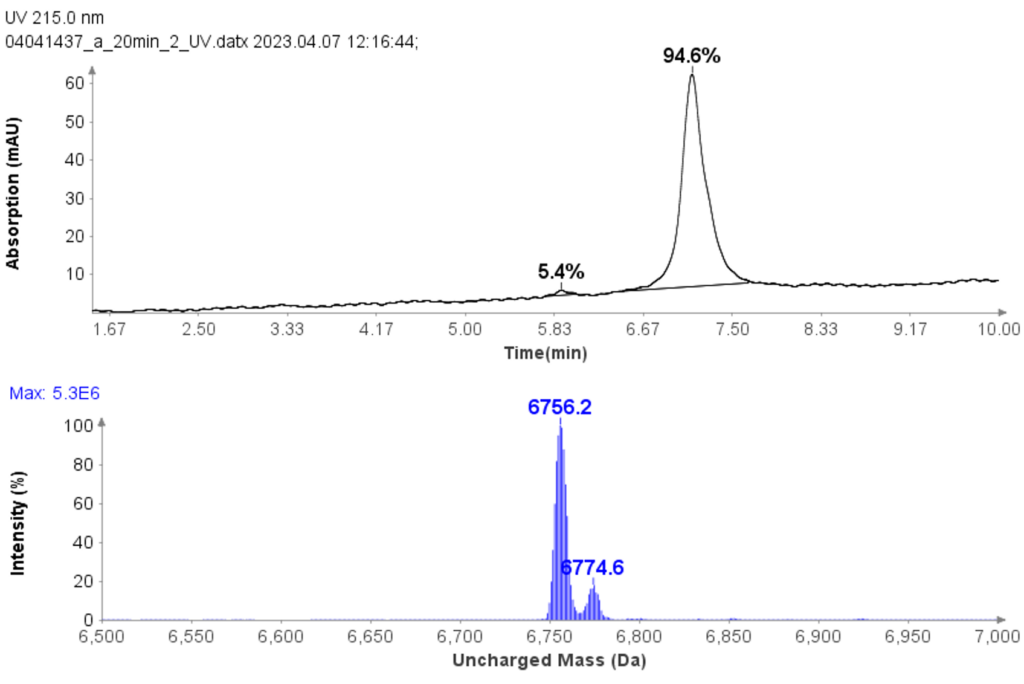
图5: (a) 18-22 的合并级分的 HPLC-UV 色谱图。 (b) CMPa 的解卷积不带电质量。
最终的总体纯度估计约为。 90%,对于药物发现中的生物活性分子来说具有极高的价值。
通过选择性馏分可以进一步提高纯度——但代价是产量。 例如,CMPa 级分 20 的 HPLC-UV/MS 分析(图 6a)显示 UV 纯度为 99.0%(图 6d),并且 MS 分析中没有氧化副产物。
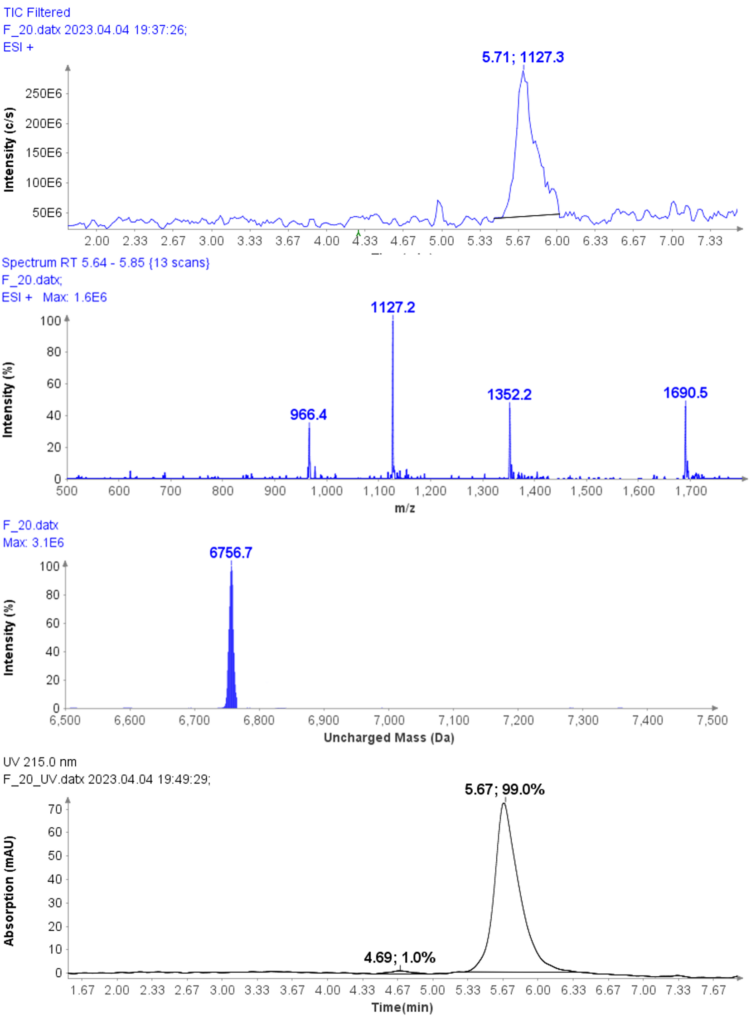
图6: (a) 馏分 20 的 HPLC-MS 色谱图,(b) 室温 5.71 分钟时峰的平均 MS 谱图,(c) CMPa 的解卷积不带电质量 (d) 馏分 20 的 HPLCUV 色谱图。
结语
puriFlash® 5.250 PrepLC/Flash 系统,与 ex 在线耦合expression® CMS 检测器具有出色的性能,有助于以高置信度从复杂基质中选择性纯化生物活性大肽。 与 UV 或 ELSD 检测器相比,质谱仪具有卓越的选择性和灵敏度。
该方法的一个说明性应用显示了酪蛋白二醇大肽的分离,通过高产率的组合级分,获得了 80% (CMPb) 至 90% (CMPa) 的纯度范围。 通过选择性馏分,可以实现高达 99.0% 的更高纯度。
参考文献:
[1]格拉斯伦德,S.,等人。 (2008)。 蛋白质生产和纯化。 自然方法,5(2), 135-146。
[2]生物制药加工:制造工艺的开发、设计和实施。
[3]林T.,等人。 (2021) 牛奶中的生物活性物质:化学、技术和应用营养评论 v79(S2):48–69
[4]Saito T.,呃。 (1991)从甜奶酪乳清中分离酪蛋白糖肽的新方法。 J.乳制品科学。 74、2831-2837
